Лептины что это такое и где вырабатываются
Лептин: влияние на липидный обмен
Молекула лептина представляет собой трехмерную структуру из 167-аминокислот, имеющую четыре антипараллельные α-спирали, которые связаны двумя длинными перекрестными звеньями и одной короткой петлей, образующей левосторонний спиральный пучок, образующий двухслойную упаковку. Дисульфидная связь между двумя остатками цистеина (Cys96 и Cys146) на С-конце лептина и в начале одной из петель важна для правильного сворачивания структуры и связывания рецептора. Мутация любого из остатков цистеина делает белок биологически неактивным.
Структуру лептина, влияющую на биологическую активность in vivo и активность связывания с рецептором in vitro, можно разделить на три типа:
(1) N-концевая аминокислотная последовательность (22–115), которая важна для биологической активности и активности связывания рецептора;
(2) C-концевая аминокислотная последовательность (116–166) с петлевой структурой, которая также важна для усиления активности N-концевой области;
(3) С-концевая дисульфидная связь, которая не нужна для активности лептина.
Лептин контролирует определенные группы нейронов в гипоталамусе, стволе мозга и других областях ЦНС. Высокая экспрессия LRb присутствует в дугообразных, дорсомедиальных, вентромедиальных и вентральных премамиллярных ядрах гипоталамуса, умеренная экспрессия LRb присутствует в перивентрикулярной области и заднем ядре гипоталамуса, а низкие уровни LRb выражены в паравентрикулярном ядре (PVN) и латеральной области гипоталамуса. (LHA). LRb также локализуется в солитарном ядре, латеральном парабрахиальном ядре, моторных и сенсорных ядрах и областях ствола мозга, которые обычно не связаны с энергетическим балансом. Повышение уровня лептина напрямую подавляет орексигенный пептид, нейропептид Y (NPY) и родственный агути пептид (AGRP) в дугообразном ядре. Гормон, концентрирующий меланин (MCH), и орексины, экспрессируемые в LHA, косвенно подавляются лептином. Лептин увеличивает уровни аноректических пептидов, α-меланоцит-стимулирующего гормона (α-MSH), производного от проопиомеланокортина (POMC), и транскриптов, регулируемых кокаином и амфетамином, продуцируемых нейронами в латеральном дугообразном ядре. Этот проект в PVN вызывает повышение уровня кортикотропин-рилизинг-гормона, тиреотропин-рилизинг-гормона и окситоцина. Чистое действие лептина заключается в подавлении аппетита, стимуляции термогенеза, усилении окисления жирных кислот, снижении уровня глюкозы и уменьшении массы тела и жира. Подавление AGRP лептином ослабляет антагонизм α-MSH посредством AGRP к рецептору меланокортина-4. Важность этих центральных нейронных цепей была подтверждена с помощью нейроанатомических и генетических методов.
Циркулирующий лептин проникает через гематоэнцефалический барьер и опосредует свое действие через сигнальный преобразователь и активатор пути транскрипции (STAT) (JAK-STAT3) киназы Януса (JAK). Связывание лептина с LRb приводит к аутофосфорилированию JAK1 и 2, тирозилфосфорилирование цитоплазматического домена LRb приводит к фосфорилированию и активации STAT3. Тирозил-фосфорилированный STAT3 подвергается гомодимеризации, перемещается в ядро и регулирует экспрессию нейропептидов и других генов.
Адипонектин представляет собой широко экспрессируемый адипокин, который проявляет мощный инсулино-сенсибилизирующий эффект за счет связывания со своими рецепторами AdipoR1 и AdipoR2, что приводит к активации AMPK, PPAR-α и, вероятно, других, еще неизвестных сигнальных путей. При резистентности к инсулину, связанной с ожирением, снижается регуляция рецепторов как адипонектина, так и адипонектина. Антидиабетические TZD могут быть интересной терапевтической стратегией при инсулинорезистентности. Новый индекс чувствительности к адипонектину (SA), определяемый как процентное соотношение HMW-формы / общего циркулирующего адипонектина, может стать важным параметром системной чувствительности к инсулину. Лептин служит основным «адипостатом», подавляя потребление пищи и способствуя расходу энергии. Лептин улучшает периферическую (печеночные и скелетные мышцы) чувствительность к инсулину и модулирует функцию β-клеток поджелудочной железы. Резистентность к лептину связана со снижением опосредованной лептином передачи сигналов JAK– STAT и индукцией супрессора передачи сигналов цитокинов-3 (SOCS-3).
Лептин – гормон похудения и как его активировать
Вы наверняка слышали эту популярную фразу: «Чтобы похудеть, надо меньше есть и больше двигаться».
Однако с точки зрения науки эта схема давно устарела, поскольку она не учитывает работу гормона лептина, без учета которого невозможно разобраться в том, по какому принципу тело накапливает и расщепляет жир.
Почему здоровый человек никогда не потолстеет?
Каждый человек, страдающий лишним весом, депрессией и постоянным чувством голода, мечтает о волшебной таблетке, которая чудесным образом избавит его от жировых отложений и вмиг сделает бодрым, полным сил и счастливым.
Но мало кто знает, что естественный механизм избавления от лишнего жира заложен в нас самой природой. Надо лишь правильно настроить его.
Расход калорий и постоянная масса тела главным образом регулируется гормоном, который называется лептин. При переедании он «заставляет» человека активнее двигаться, тем самым, способствуя активации процесса расщепления жира. А при недостаточном объеме пищи лептин «замедляет» этот процесс, соответственно снижая и физическую активность. Таким образом, получается, что лептин сам справляется со своей задачей, и подсчитывать калории специально вовсе необязательно.
Что такое лептин?
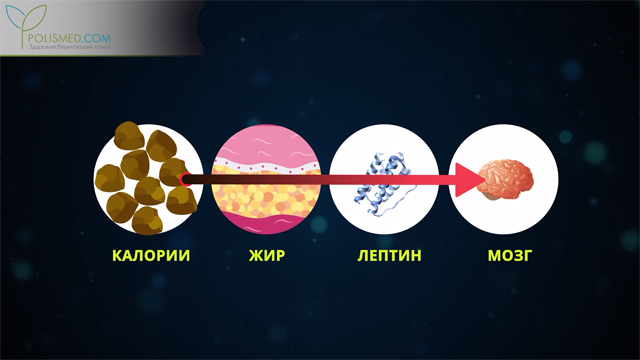
Гормон лептин был открыт в 1994 году и с тех пор перевернул представление ученого мира о жировой массе в организме человека. Оказалось, что жир не лежит «мертвым грузом» в нашем теле. Он обладает гормональной активностью – выделяет тот самый гормон лептин. Этот гормон собирает информацию об энергетических ресурсах организма и сообщает ее в мозг, который затем принимает решение, как ее тратить.
Лептин влияет не только на расход энергии и сжигание жиров, но и определяет наше поведение, мотивацию, настроение и даже половую активность.
Нарушение в работе этого гормона является главной причиной ожирения. В этой статье мы расскажем, как наладить работу лептина.
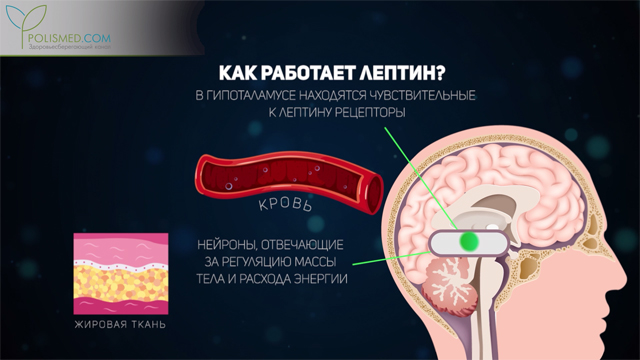
Как работает лептин?
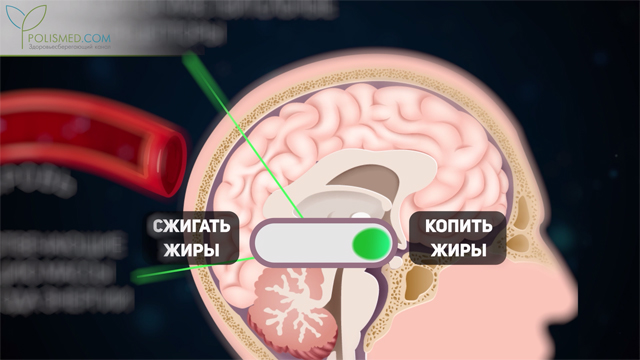
Лептин вырабатывается в жировой ткани, откуда поступает в кровь, посредством которой попадает в мозг, достигая, в итоге, гипоталамуса, где расположены чувствительные к нему рецепторы и нейроны, которые отвечают за расход организмом энергии, а также за массу тела. Лептин играет роль «переключателя», дающего команду либо сжигать жиры, либо накапливать их.
Два режима нашего организма
Что происходит, когда мы переключаем скорости в автомобиле? Мы постепенно увеличиваем подачу топлива в двигатель. На первой скорости автомобиль едет очень медленно, а на пятой мчится на всех парах.
Наш организм устроен гораздо сложнее, но он также расходует энергию с разной скоростью, а точнее, в двух разных режимах – в режиме изобилия или в режиме дефицита.
«Переключение» между этими двумя режимами происходит в гипоталамусе, причем непосредственно под воздействием лептина.
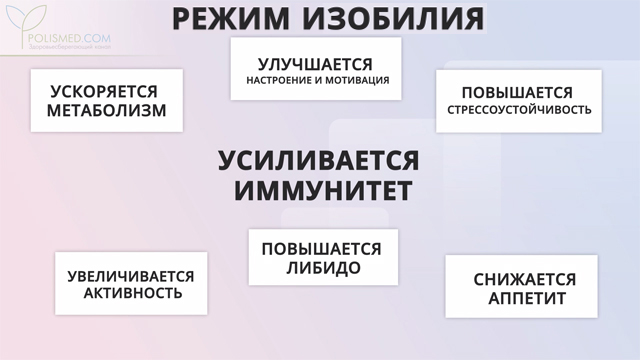
Режим изобилия
В этом режиме энергия расходуется по максимуму. В норме он наступает, когда мы потребляем больше калорий, чем тратим. Избыточные калории откладываются в виде жира, вследствие чего в крови повышается уровень лептина. А лептин, в свою очередь, сообщает мозгу о необходимости расхода лишних запасов.
В режиме изобилия происходит следующее:
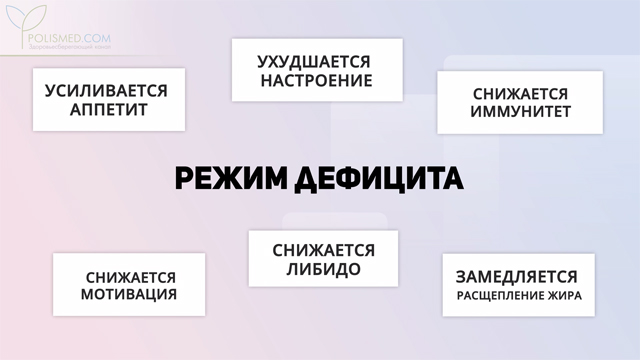
Режим дефицита
Когда мы тратим больше калорий, чем потребляем с едой, уровень лептина в нашей крови падает. Мозг расценивает это как начало трудных времен и переключает расход энергии в режим дефицита, заставляя организм существовать под девизом «выжить любой ценой».
Это полная противоположность режиму изобилия.
В режиме дефицита происходит следующее:
Режим дефицита – это древнейшая функция нашего организма, которая не раз спасала жизнь нашим далеким предкам. Чувствуя наступление голодных времен, мы буквально цепляемся за каждую калорию, а мозг, можно сказать, кричит нам в ухо: «Не шевелись! Не совершай ни единого движения без крайней необходимости! Экономь энергию!».
Интересный факт!
Режим дефицита доступен не только человеку, но и всем млекопитающим. Например, зимняя спячка у медведя – это не что иное как медвежий вариант режима дефицита. Согласно одной из теорий, именно благодаря этой функции млекопитающие пережили динозавров.
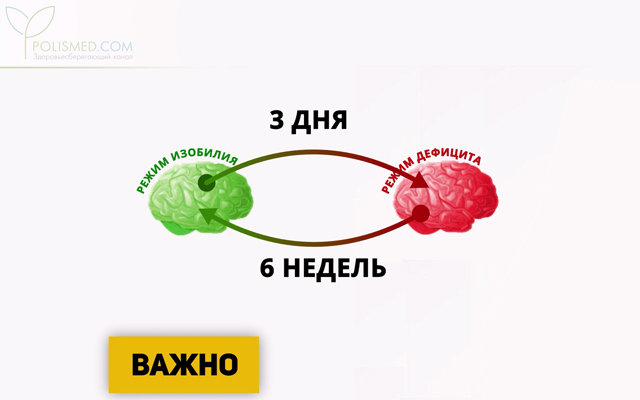
Важно!
Переход от режима изобилия к режиму дефицита занимает всего 3 дня. Обратный переход может занять целых 6 недель.
Сбой в работе гормона лептина
Лептинорезистентность – это гормональный сбой, из-за которого мы толстеем.
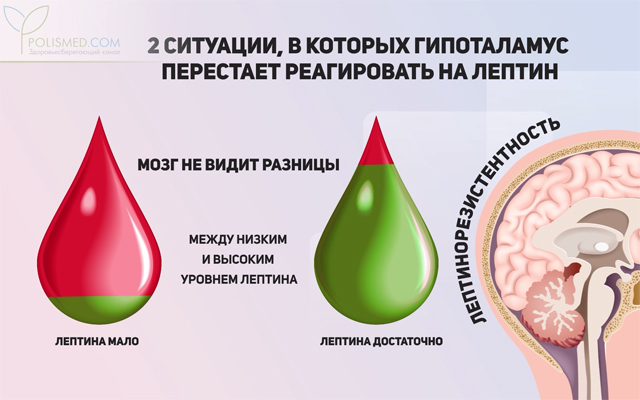
Есть две ситуации, в которых гипоталамус перестает реагировать на лептин.
Проблема в том, что мозг «не видит» разницы между низким и высоким уровнем лептина. Когда рецепторы гипоталамуса по любым причинам не реагируют на лептин, мозг расценивает это как начало «голодных времен» и начинает функционировать в режиме дефицита.
Итак, представьте себе ситуацию, когда у человека развилась нечувствительность к лептину. Он хорошо питается, у него увеличивается жировая прослойка, а значит, повышается уровень лептина. Но организм не «включает» режим изобилия, чтобы сжечь лишние калории, поскольку мозг не реагирует на лептин, и продолжает жить в режиме дефицита.
Возникает парадоксальная ситуация. Человек хорошо питается, жировые запасы растут, но организм работает в таком режиме, будто он попал в блокадный Ленинград.
Соответственно, появляются все «прелести» режима дефицита:
Причины лептинорезистентности
Причины нечувствительности к лептину, приводящие к ожирению, необходимо знать каждому. Подразделить их можно на два основных вида – физиологические факторы и пищевые факторы.
К физиологическим факторам относятся:
К пищевым факторам относятся:
Важно!
Женщины чаще сталкиваются с лептинорезистентностью, причем нередко создают ее собственными усилиями. Из-за современной моды на худобу многие женщины критически относятся к своей естественной полноте и практикуют скудную диету в сочетании с высокими физическими нагрузками. Такая практика буквально может сломать метаболизм, вызвав потерю чувствительности организма к лептину.
Порочный круг ожирения
Под воздействием одного из перечисленных факторов в организме развивается воспалительная реакция. Во время воспаления в крови повышается С-реактивный белок или СРБ.
Исследования на мышах показали, что СРБ блокирует действие лептина. Проще говоря, лептинорезистентность – это сочетание повышенного лептина и С-реактивного белка.
Более того, повышенный лептин усиливает продукцию СРБ клетками печени. Формируется замкнутый круг, то есть, чем больше лептина, тем больше СРБ, и тем сильнее он блокирует действие лептина.
В итоге у человека постепенно развивается ожирение. А, согласно последним научным данным, любое ожирение сопровождается хроническим воспалением, протекающим в жировой ткани. Таким образом, следствие стимулирует свою причину. Круг замыкается – человек продолжает оставаться в режиме дефицита, а естественный механизм расщепления жира не работает годами.
Лептин и печень
Огромное количество хронических болезней начинаются именно с нарушения функциональности печени, и наука все чаще подтверждает это.
Накопление жира в этом органе носит название неалкогольной жировой болезни печени. Это одно из самых распространенных хронических заболеваний в развитых странах (например, около 30% взрослого населения Европы и Америки страдают этой болезнью).
При этом заболевании уровень лептина в организме повышается, и человек, как правило, страдает от ожирения. Но так происходит не всегда.
Врачи говорят: «Вас можно считать жирным, если у Вас жирная печень. При этом внешне Вы можете быть худым».
Как развивается жировая болезнь печени?
Все начинается с плохого питания. Неправильный рацион становится причиной накопления в печени, так называемого, висцерального жира. Когда его количество в печени превышает критический уровень, начинают выделяться воспалительные белки, которые блокируют работу лептина, провоцируя ожирение.
Повышенный лептин, в свою очередь, усугубляет течение жировой болезни печени. Это еще один порочный круг, вызванный сбоем в работе лептина.
Важно!
Если человек страдает ожирением, то у него практически всегда наблюдаются и проблемы с печенью. Если у Вас обнаружили жировую болезнь печени, не отчаивайтесь. При грамотном подходе это состояние полностью обратимо.
Лептины что это такое и где вырабатываются
Понимание конкретной биологической роли эффекторных молекул нашего организма имеет не только теоретическую ценность, но и важное практическое значение, заключающееся в возможности их использования в качестве биомаркеров и мишеней для терапевтического воздействия [1–3]. В последнее время, благодаря усовершенствованию молекулярно-генетических технологий, методов белкового анализа, открывается множество различных регуляторных соединений, которые не только меняют наше представление о функционировании органов и тканей, но и создают предпосылки для улучшения лечебно-профилактических стратегий [4, 5]. К числу молекул, имеющих большие перспективы для практического здравоохранения, относится белок лептин.
Целью этой статьи является систематизация существующих данных о биологической роли лептина. В статье нами последовательно будут рассмотрены следующие аспекты: генетика и биология лептина, сигнальный путь и механизм действия лептина, регуляция образования лептина, а также функции лептина в норме и при патологических процессах.
Лептин (в переводе с греч. leptos – тонкий) – гормон пептидной природы, выделяемый адипоцитами. Открытие лептина Y. Zhang с соавт. в 1994 г. вызвало большой интерес в плане дальнейшего изучения гормональной функции жировой ткани [6, 7]. Первоначально открытый лептин также назвали «белок ob» (сокращенно от obese, англ. – страдающий ожирением). Ген, кодирующий образование лептина, также первоначально был назван «геном ob» (сейчас чаще используется термин «ген LEP»), он расположен на хромосоме 7q31.31. С момента открытия лептина сформировалась новая концепция о функционировании жировой ткани, согласно которой она действует как активный эндокринный орган, помимо инертного органа хранения липидов и энергии, как считалось ранее [6–8]. Лептин состоит из 167 аминокислот и вырабатывается преимущественно белой жировой тканью нашего организма. Считается, что общая концентрация лептина, циркулирующего в организме, равна общему количеству жира человека. Первоначальные исследования показали, что лептин может играть определенную роль в контроле избыточного набора жира в нашем организме, но впоследствии стало известно, что большее высвобождение лептина приводит к большему потреблению пищи и накоплению жира. Лептин также вырабатывается плацентой и желудком, но гораздо в меньшем количестве по сравнению с жировой тканью [9, 10]. Лептин, имеющий молекулярную массу 16 кД, действует в головном мозге через нейронные гипоталамические пути и таким образом регулирует энергетический гомеостаз [8]. Исследования показали, что дефицит лептина приводит к ожирению, что объясняет его роль в потреблении пищи, использовании энергии, репродукции, функциях щитовидной железы и иммунитете [11]. Несколько исследований также показали, что лептин вызывает окисление жиров у людей с ожирением [12]. Благодаря широкому разнообразию функций лептина, исследователи предприняли усилия, чтобы продемонстрировать и прояснить его роль с биологической точки зрения.
Генетика и биология лептина
Ген лептина был первоначально обнаружен с помощью метода поиска, ассоциированного с болезнью гена мышей ob/ob, и поэтому его также называют «геном ob». Этот ген экспрессируется в белой жировой ткани, желудке, плаценте и, возможно, в молочной железе. Он относится к семейству цитокинов, так как имеет кристаллическую структуру [6, 13]. Лептин, будучи гормоном, имеет циркадные (суточные) вариации концентрации с повышенным уровнем, обнаруживаемым вечером, и импульсной секрецией в ранние утренние часы. Поскольку он преимущественно продуцируется адипоцитами, его основная роль заключается в регулировании энергетического гомеостаза, который включает в себя потребление пищи, использование энергии и регулирование массы тела. Он также играет другие важные функции, такие как регулирование иммунных и воспалительных реакций, вызывая ангиогенез и заживление ран. Из-за своей роли в энергетическом гомеостазе и регулировании массы тела его также называют «гормоном против ожирения» или «гормоном похудения» [14, 15]. Помимо этого, исследования показали, что лептин играет важную роль в формировании высокого кровяного давления у людей с ожирением [14, 16, 17].
Сигнальный путь и действие лептина
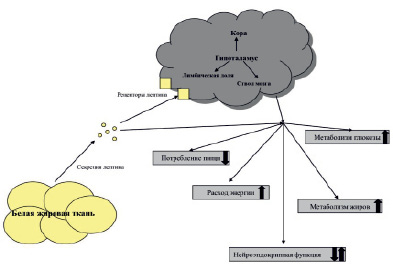
Лептин оказывает свое действие, связываясь с рецептором лептина (LEP-R или OB-R), который у человека кодируется геном LEPR. LEP-R обнаруживается во многих областях мозга и эндотелии мозговых капилляров. LEP-R входит в состав семейства цитокиновых рецепторов гликопротеина 130. После соматической рекомбинации LEP-R были сгенерированы различные изоформы рецептора лептина, из которых LEPEb является наиболее важной и самой длинной изоформой, вызывающей сильный сигнальный путь. Исследования сообщили о мутациях в LEPR, которые вызывают ожирение. После связывания с LEPR лептин осуществляет сигнальный каскад через Янус-киназу (JAK), сигнальный преобразователь и активатор транскрипции (белок STAT). В некоторых исследованиях было показано, что лептин активирует путь STAT3 в гипоталамической области мозга (рис. 1) [18–20].
Рис. 1. Эффекты лептина. Примечание. Лептин действует либо напрямую, либо путем активации определенных центров в центральной нервной системе для уменьшения потребления пищи, увеличения расхода энергии, влияния на метаболизм глюкозы и жиров или изменения нейроэндокринной функции
Регуляция образования лептина
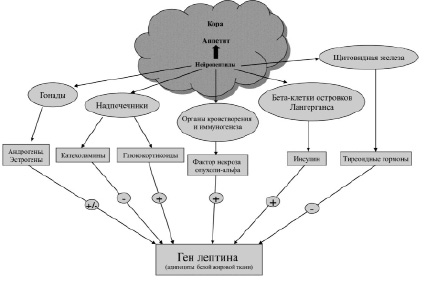
Регуляция образования лептина происходит многими гормонами в организме человека в виде увеличения или уменьшения его синтеза на клеточном уровне. Инсулин увеличивает синтез лептина, в то время как адреналин, норадреналин и дофамин снижают синтез лептина. Помимо этих факторов, фактор некроза опухоли-α также увеличивает секрецию лептина (рис. 2). Глюкоза и жирные кислоты также влияют на экспрессию лептина и, в свою очередь, на его секрецию [21–23].
Рис. 2. Регуляция образования лептина. Примечание. Лептин после высвобождения из адипоцитов связывается с рецепторами лептина в гипоталамусе и изменяет экспрессию нескольких нейропептидов; они, в свою очередь, снижают аппетит, увеличивают расход энергии за счет изменения симпатического и парасимпатического тонуса и изменяют нейроэндокринную функцию. Повышение уровня лептина активирует оси щитовидной железы, гормона роста и гонад и подавляет ось гипофиз – надпочечник. Лептин, действуя прямо или косвенно (изменяя уровни других гормонов и нейропептидов), также влияет на кроветворение и иммунную функцию и улучшает метаболизм глюкозы и жиров. Наконец, измененная продукция и уровни циркуляции гормонов и цитокинов влияют на выработку лептина адипоцитами: + – стимулирующее действия, – – ингибирующее действие
Биологическая роль лептина
Согласно результатам многочисленных клинических и экспериментальных исследований лептин выполняет в организме человека множество важнейших функций, а именно: регуляцию обмена липидов, регуляцию энергетического гомеостаза, регуляцию нейроэндокринных функций, регуляцию обмена углеводов, играет важную роль в развитии новорожденных, детском возрасте и в периоде полового созревания, а также принимает участие в метаболизме сердечно-сосудистой системе, костной ткани и иммунных реакциях [23–25]. Такая многогранная роль лептина делает его весьма ценным и перспективным объектом дальнейших исследований с целью возможностей использования в качестве раннего биомаркера и в качестве лекарственного препарата.
Роль лептина в регуляции энергетического гомеостаза
Лептин играет важную роль в энергетическом гомеостазе, регулируя аппетит. Лептин активирует сложную нейрональную петлю, состоящую из анорексигенных нейронов (т.е. снижающих аппетит), которые высвобождают проопиомеланокортин (POMC), и орексигенных нейронов (т.е. стимулирующих аппетит), которые высвобождают нейропептид Y (NPY), регулирующий потребление пищи. Недавний метаанализ показал, что состояние натощак и диета с ограничением калорий до половины от общей потребности могут значительно снизить уровень лептина. Клинически мутация в гене лептина или его рецепторе приводит к ожирению из-за гиперфагии. Исследования показали, что введение лептина таким пациентам снижает потребление пищи за счет повышения сытости [24–26].
Роль лептина в регуляции нейроэндокринной функции
Уровень лептина падает во время голодания, и это не зависит от жировой массы. Голодание приводит к нейроэндокринным реакциям как у человека, так и у мышей, что включает в себя снижение уровня гормонов, важных для размножения. Это, в свою очередь, уменьшает изменения во время беременности (энергозатратный процесс), снижает уровень гормонов, высвобождаемых из щитовидной железы, что замедляет скорость метаболизма, повышает уровень гормона роста, который может участвовать в перемещении запасов энергии в организме и может замедлять деятельность, связанную с ростом. Но исследование показало, что пациент, у которого имеется дефицит лептина с рождения, может иметь нормальный рост и развитие организма, а также нормальное функционирование надпочечников, в отличие от того, что было замечено в экспериментах у мышей [27, 28].
Роль лептина в регуляции обмена углеводов. Инсулинорезистентность и метаболический синдром
Мутация гена лептина, наблюдаемая у мышей ob/ob и мышей db/db, а также генетический дефицит лептина, наблюдаемый у человека, показали резистентность к инсулину и некоторые особенности метаболического синдрома. Лечение лептином корригировало гиперинсулинемию, гипергликемию до потери веса как у мышей, так и у человека. Но у человека он также снижал уровень триглицеридов, холестерина и липопротеинов низкой плотности (ЛПНП) и повышал уровень липопротеинов высокой плотности (ЛПВП) [29]. Лептин также был вовлечен в воспаление, обнаруженное у тучных женщин, которое может привести к гестационному сахарному диабету (ГСД). Лептин не только контролирует баланс между насыщением и энергией матери, но и вырабатывается плацентой, которая, в свою очередь, поддерживает жизнеспособность плода. Основным источником циркулирующего лептина у матери является его плацентарная продукция, которая мобилизует жир у матери, усугубляя вероятность возникновения ГСД. При ГСД лептин оказывает значительное влияние на плаценту аутокринным/паракринным способом. Это приводит к увеличению размеров плаценты, облегчает перенос плацентарных питательных веществ через глицериновый транспортер и аквапорин-9 и увеличению размеров плода (макросомия). В основном инсулинорезистентность может усугублять течение ГСД и способствовать повышению уровней лептина в плазме крови при ГСД, а дальнейшее воспаление, связанное с ожирением, играет свою собственную роль в развитии инсулинорезистентности. Поэтому для лечения ГСД рассматриваются питательные вещества, обладающие противовоспалительным действием.
Ожирение с инсулинорезистентностью участвует в обострении синдрома поликистозных яичников (СПКЯ), при котором исследования выявили более высокий уровень лептина. Недавнее исследование продемонстрировало индукторный эффект лептина при иммунном дисбалансе, наблюдаемом при СПКЯ, за счет индукции интерферона-γ (INF-γ), который может участвовать в апоптозе гранулезных клеток [30, 31].
Роль лептина в регуляции метаболизма сердечно-сосудистой системы и сердечно-сосудистых заболеваниях (ССЗ)
Роль лептина в развитии и метаболизме ССЗ до конца не изучена. Несколько экспериментальных исследований на животных моделях, таких как диабетические (db/db) и тучные (ob/ob) модели, отчетливо показали благотворную роль лептина в регуляции сердечного метаболизма. При нормальных физиологических условиях сердце использует глюкозу и жир в качестве источника энергии, но предпочтительно глюкозу. В моделях животных с дефицитом лептина или LEP-R нарушается регуляция сердечного метаболизма путем перехода на повышение использования жиров вместо обычного предпочтительного использования глюкозы. Это приводит к повышенному окислению жира, увеличению потребления кислорода миокардом и снижению сердечной деятельности, что в конечном итоге приводит к системным метаболическим нарушениям, таким как инсулинорезистентность, резистентность к лептину и метаболическая дисфункция. Кроме того, повышенные уровни триглицеридов и накопление жира в миокарде на таких животных моделях приводили к липотоксичности, которая, в свою очередь, влияет на сократительную способность сердца [22, 32]. Таким образом, исследования, проведенные на животных моделях, показывают, что лептин может защитить сердце от накопления липидов и липотоксических эффектов, действуя как антилипотоксическое средство.
В различных исследованиях наблюдались противоречивые результаты относительно связи лептина с ишемической болезнью сердца (ИБС) и хронической сердечной недостаточностью (ХСН). Повышенный уровень лептина был связан с риском развития ИБС и ХСН. Однако терапия, снижающая уровень лептина, может способствовать снижению сердечно-сосудистого риска у таких пациентов. Сообщалось, что более высокие уровни лептина предсказывают риск развития инсульта, атеросклеротическое поражение сонных артерий и заболевания периферических артерий (ЗПА). Также сообщалось, что гиперлептинемия ускоряет рост аневризмы брюшной аорты, но для установления четкой связи требуются дальнейшие исследования [22, 33, 34].
Роль лептина у новорожденных
Плацента выделяет лептин в пуповинную кровь, что имеет большое значение для новорожденных. Было установлено, что уровни лептина положительно связаны с общей массой тела и жировой массой новорожденного. Помимо энергетического гомеостаза, лептин регулирует рост, способствует кроветворению и лимфопоэзу в неонатальном периоде. Секреция лептина с молоком также позволяет предположить, что уровень лептина у матери может влиять на рост новорожденных младенцев [35–37].
Роль лептина в детском возрасте и при половом созревании
В детском возрасте и периоде полового созревания лептин посылает сигнал в мозг для накопления жиров, за счет чего в конечном итоге регулирует пубертатные изменения, менструальный цикл и репродукцию. В начале полового созревания увеличение жировой массы тела происходит из-за повышенного уровня лептина у нормальных детей, что, в свою очередь, предполагает, что он вызывает половое созревание у людей. Напротив, лица с мутациями в гене LEPR страдают ожирением, остаются препубертатными и имеют гипогонадотропный гипогонадизм [38–40].
Роль лептина в метаболизме костной ткани и воспалении
Известно, что лептин играет важную роль при ревматических заболеваниях и остеоартрите. Уровень лептина повышен у больных остеоартритом. Большинство исследований выявили катаболическую роль лептина в хрящах. Роль лептина при этих заболеваниях также предполагает, что он действует как провоспалительный фактор на метаболизм хряща. Лептин рассматривается не только как медиатор воспаления при аутоиммунных заболеваниях, но и при других воспалительных заболеваниях [41, 42]. В противоположность этому, хронические воспалительные состояния, вторичные по отношению к метаболическим, аутоиммунным или инфекционным заболеваниям, могут привести к резистентности к лептину, за которой последует развитие ожирения, которое, в свою очередь, потенцирует воспаление [42–44].
Роль лептина в иммунных реакциях
Лептин регулирует как естественные, так и приобретенные иммунные реакции. Что касается врожденного иммунитета, лептин увеличивает силу естественных киллеров (NK) клеток и способствует активации гранулоцитов, макрофагов и дендритных клеток [45–47]. Что касается адаптивного иммунитета, лептин увеличивает размножение новообразованных Т- и В-лимфоцитов, в то же время он уменьшает размножение регуляторных Т-клеток (Т-супрессоров). Таким образом, лептин активирует В-лимфоциты, которые секретируют цитокины для контроля продукции и созревания Т и В-лимфоцитов [48, 49].
Заключение
Таким образом, лептин, или белок ob, является гормоном, который преимущественно продуцируется адипоцитами белой жировой ткани и реагирует с рецептором лептина, который, в свою очередь, инициирует сигнальный каскад по пути JAK-STAT. Передача сигналов лептина активирует выработку различных нейропептидов, таких как проопиомеланокортин и нейропептид Y, что приводит к снижению и увеличению аппетита соответственно. Уровень лептина в крови отражает общее количество запасов энергии в жировой ткани, а это, в свою очередь, направляет центральную нервную систему на регулирование энергетического гомеостаза, нейроэндокринных функций, метаболической регуляции, роста новорожденных, ряда изменений в детском и половом возрасте. Дефицит лептина может быть обусловлен либо мутацией в гене лептина, либо наследственной липоатрофией. Дефицит лептина приводит к нарушениям многих важнейших функций, в частности вызывает репродуктивную недостаточность, ожирение, инсулинорезистентность, сахарный диабет, метаболический синдром и аутоиммунные заболевания. Дальнейшее изучение и уточнение биологической роли лептина является актуальным научно-исследовательским направлением для улучшения ранней диагностики и разработки лечебно-профилактических мероприятий при данных нозологиях.