Лучевой эпителиит что это
РАДИОЭПИТЕЛИИТ
Р. может развиться при лучевой терапии (см.), случайном попадании радионуклидов на слизистую оболочку, кишечной форме лучевой болезни (см.).
Патогенез Р. связан с повреждением клеточных элементов эпителия вследствие нарушения кровообращения и лимфообращения и трансмембранного обмена веществ, присоединения вторичной инфекции.
Радиочувствительность слизистой оболочки различных органов неодинакова (см. Радиочувствительность). Наиболее радиочувствительна слизистая оболочка полости рта, тонкой кишки, мочевого пузыря; менее чувствительна к воздействию ионизирующего излучения слизистая оболочка прямой кишки, влагалища, матки. Наличие воспалительных явлений, отека и сопутствующих заболеваний увеличивают опасность лучевого повреждения слизистой оболочки.
Скорость развития и выраженность Р. зависят от дозы ионизирующего излучения, поглощенной слизистой оболочкой (см. Дозы ионизирующих излучений, Критические органы), объема облучаемых тканей, энергии излучения (см. Ионизирующие излучения), фракционирования дозы (см. Фактор времени облучения). Чем больше объем облучаемой ткани, разовые дозы облучения и короче срок, в течение к-рого проводят лучевую терапию, тем более вероятен риск развития Р. При увеличении энергии ионизирующего излучения опасность возникновения Р. может уменьшиться.
По тяжести клин, проявлений различают катаральный и эрозивный Р. Катаральный Р. — лучевая реакция, сопровождающая в большинстве случаев лучевую терапию опухолей. При катаральном Р. характерны отек и гиперемия слизистой оболочки, появляются болезненные ощущения. При облучении опухолей полости рта наблюдается сухость слизистой оболочки, чувство жжения во рту, потеря вкусовых ощущений; при облучении пищевода и глотки — болезненность при глотании. Реакция со стороны кишечника сопровождается снижением аппетита, вздутием живота, разлитой болезненностью, усилением перистальтики, частым стулом и наличием жидких испражнений со слизью. При катаральном ректите присоединяются тенезмы и боли при дефекации. При облучении зоны мочевого пузыря отмечается учащенное болезненное мочеиспускание.
Эрозивный Р. — раннее осложнение лучевой терапии, развивающееся в течение первых 6 мес. от начала лечения и сопровождающееся отторжением эпителия на фоне отека и гиперемии слизистой оболочки. Исходом эрозивного Р. является атрофия слизистой оболочки и под-слизистой ее основы с нарушением местного кровообращения, на фоне которых могут возникать поздние лучевые осложнения язвенного характера.
Лечение Р. включает использование дегидратационных и противовоспалительных средств, профилактику вторичной инфекции, стимуляцию регенераторных процессов. Применяют растительные масла, антибактериальные средства, поливитамины. При ректитах и циститах — свечи с метилурацилом (метацилом), микроклизмы из рыбьего жира и настоя ромашки, введение в мочевой пузырь метилурацила (метацила) и димексида.
Прогноз, как правило, благоприятный. Однако в последующем в зоне Р. могут развиться язвенно-некротические процессы, приводящие к рубцеванию и стенозированию полых органов.
Библиография: Козлова А. В. Возможные последствия повреждений органов и тканей при лучевой терапии злокачественных опухолей, Мед. радиол., т. 22, № 12, с. 71, 1977; Bosaeus I., AnderssonH. а. N у s t г ö m C. Effect of low-fat diet on bile salt excretion and diarrhoea in the gastrointestinal radiation syndrome, Acta radiol. Oncol. Radiat. Phys. Biol., v. 18, p. 460, 1979; WeghauptK. u. Kucera H. Zur strahlentherapeutischen Behandlung des Gebärmutterhalskarzinoms unter besonderer Berücksichtigung der Strahlenfolgen am Darm, Strahlentherapie, Bd 156, S. 78, 1980.
Реабилитация после лучевой терапии
Лучевая терапия играет важнейшую роль в лечении злокачественных новообразований различной локализации.
Лучевая терапия играет важнейшую роль в лечении злокачественных новообразований различной локализации. Она может использоваться как полностью самостоятельный метод или в комплексе с хирургическим лечением и химиотерапией.
Ионизирующее излучение — это энергия, которая высвобождается атомами веществ в виде элементарных частиц или электромагнитных волн. Мы сталкиваемся с этим явлением ежедневно, поскольку существует естественный радиационный фон, источниками которого являются десятки радиоактивных элементов, находящихся в почве, воде и воздухе.
Помимо естественного излучения человек периодически сталкивается с искусственным. Пример такого воздействия — это флюорография, которую необходимо проходить ежегодно. Повреждающее действие, которое радиация может оказывать на биологические ткани, используется в радиотерапии злокачественных новообразований.
Воздействие на биологические ткани
Когда ионизирующее излучение проникает в клетку, оно вызывает разрыв химических связей в веществах, в результате чего клеточные структуры перестают правильно выполнять свою работу. В клетке нет структур, которые устойчивы к радиации, хотя их восприимчивость к ней отличается, а выраженность изменений зависит от дозы облучения.
Одной из ведущих причин гибели клетки является повреждение генетического аппарата. В одних случаях клетка погибает сразу, в других пытается восстановиться, но повреждение ДНК приводит к тому, что ее потомство после нескольких циклов деления также погибает. Впрочем, если доза облучения оказалась недостаточной для выраженных изменений, клетка полностью восстанавливается спустя 2-6 часов.
Наиболее чувствительны к воздействию радиации те клетки, что находятся в процессе деления. Это позволяет применять радиотерапию в лечении онкологических заболеваний: растущие клетки опухоли более подвержены губительному влиянию облучения, чем здоровые ткани.
Большинство злокачественных новообразований обладают высокой чувствительностью к воздействию радиации, поэтому в странах с развитой медициной более половины онкобольных проходят курс лечения лучевой терапией на том или ином этапе. Процент таких пациентов постепенно увеличивается, поскольку современная медицина позволяет реализовать главный принцип радиотерапии — подать большую дозу облучения в опухоль, предохраняя от повреждения здоровые ткани. Новые методики дистанционной радиотерапии значительно снижают лучевую нагрузку на пациента, обеспечивая лучшую переносимость лечения. Оградить здоровые ткани от ионизирующего облучения на 100% невозможно. Поэтому у некоторых пациентов возможно возникновение тех или иных осложнений после лучевой терапии.
Осложнения после лучевой терапии
При проведении радиотерапии могут возникнуть общая лучевая реакция и местные изменения в облучаемой области.
Общая лучевая реакция
Речь идет об общей лучевой реакции на излучение. Она возникает не только вследствие повреждающего действия радиации, но и в результате интоксикации организма продуктами распада опухоли. Тяжесть реакции зависит от дозы полученной радиации и от того, какие технологии применялись при лечении.
В большинстве случаев общая лучевая реакция выражена слабо и не требует перерыва в проведении лучевой терапии или ее отмены. Основными клиническими проявлениями могут быть:
Симптомы общей лучевой реакции исчезают самостоятельно вскоре после облучения — в течение 2-4 недель.
Однако, в системе Томотерапии, при применении запатентованной технологии формирования луча, негативные побочные эффекты встречаются значительно реже, чем при применении общей лучевой терапии.
Местные лучевые осложнения
Местные реакции могут быть ранними (до 3 месяцев после облучения) и поздними (спустя много месяцев и даже лет). Их клиническая картина весьма разнообразна и зависит в первую очередь от того, какие ткани подверглись облучению:
Покраснения, радиодерматит, лучевые язвы, выпадение волос.
Язвенные изменения, воспаление гортани, глотки, нарушение слюноотделения.
Органы брюшной полости и малого таза
Лучевое повреждение с воспалением облученных сегментов и соответствующей симптоматикой: расстройство стула, ложные позывы к дефекации, дискомфорт в животе.
Органы грудной клетки
Лучевая пневмония (одышка, кашель), воспаление пищевода (дискомфорт и болезненность при прохождении пищи), перикарда.
Спинной и головной мозг
Воспалительные изменения нервной ткани.
Задержка роста костей и остеопороз.
В системе Томотерапия используется технология, минимизирующая воздействие радиации на окружающие опухоль здоровые органы и ткани, благодаря чему лечение переносится комфортно и повышается качество жизни пациента.
Абсолютное большинство представленных нарушений носит временный характер и поддается коррекции. Для предупреждения многих осложнений достаточно придерживаться несложных правил по восстановлению.
Восстановление после лучевой терапии
Для профилактики общей лучевой реакции и быстрого устранения ее проявлений пациенту рекомендуют богатое витаминами питание, достаточное потребление жидкости, ежедневные прогулки на свежем воздухе. При необходимости врач может назначить лекарственные препараты, например, противовоспалительные средства или стимуляторы кроветворения.
Коррекция местных изменений зависит от симптомов конкретного осложнения. Так, при поражении кожи назначают общеукрепляющую терапию и местные средства противовоспалительного и рассасывающего действия.
Как при проведении лучевой терапии, так и после нее, следует уделять внимание правильному питанию. Вот основные рекомендации, которые применимы к большинству пациентов, однако следует обсудить это со своим доктором:
При облучении головы и шеи могут наблюдаться сухость во рту, небольшие боли при приеме пищи, першение в горле. Чтобы смягчить эти последствия исключите из рациона все соленое, острое или кислое. Принимайте хорошо измельченную пищу с низким содержанием жиров, приготовленную на пару или вареную. Питайтесь чаще, небольшими порциями. Пейте больше жидкости, свежеприготовленные соки, но откажитесь от соков из цитрусовых. Пища должна быть комнатной температуры, чтобы в меньшей степени раздражать слизистые оболочки.
Облучение органов брюшной полости и малого таза иногда сопровождается тошнотой и рвотой, жидким стулом, потерей аппетита. В таких случаях полностью приемлемы все предыдущие рекомендации. При возникновении поноса можно исключить молочные продукты. Рекомендованы овощные супы на слабом мясном бульоне, обязательно протертые каши, кисели, картофельное и овощное пюре, паровые котлеты или из нежирного мяса, отварная рыба, свежий творог, хлеб из пшеничной муки, яйцо.
Сбалансированная диета поможет легче перенести лечение и предупредить потерю веса. Соблюдайте назначения врача, помните, что лучевая терапия поможет вам избавиться от заболевания. Современные методы лучевого лечения во многом лишены недостатков классической дистанционной радиотерапии, поскольку в них используются технологии, позволяющие уменьшить объем общего облучения, минимизируя его воздействие на здоровые ткани.
Пациенты, проходящие лечение на системе Томотерапии, подвержены меньшему количеству побочных эффектов по сравнению с пациентами, получающими обычную лучевую терапию. Лечение хорошо переносится в амбулаторных условиях.
Лечение местных лучевых повреждений
Местные лучевые повреждения, развивающиеся преимущественно при лучевой терапии злокачественных опухолей, отличаются торпидностью к лечению различными медикаментозными средствами. Лучевые повреждения покровных тканей (кожи, слизистых) и внутренних органов
Местные лучевые повреждения, развивающиеся преимущественно при лучевой терапии злокачественных опухолей, отличаются торпидностью к лечению различными медикаментозными средствами. Лучевые повреждения покровных тканей (кожи, слизистых) и внутренних органов, как следствие воздействия ионизирующего излучения в суммарной очаговой дозе 60—70 Гр., проявляются в виде хронических эпителиитов и дерматитов, с прогрессированием их в лучевые язвы кожи, лучевые проктиты, циститы и т. п. В патогенезе таких повреждений, наряду с нарушением микроциркуляции, ведущее значение играет прямое воздействие излучения на клетки и подавление репаративных процессов. В дальнейшем на передний план выходят присоединение инфекции поврежденных тканей и усугубление негативных процессов заживления поврежденных тканей [1]. Вот почему в комплекс медикаментозных средств при лечении местных лучевых повреждений включаются вещества, воздействие которых направлено на улучшение тканевой микроциркуляции, повышение репараторных процессов и подавление инфекционного процесса. Для лечения местных лучевых повреждений апробированы практически все известные медикаментозные средства, удовлетворяющие перечисленным требованиям. Низкая терапевтическая эффективность имеющихся средств явилась основанием для поиска новых методов лечения. В отделении лечения лучевых повреждений МРНЦ РАМН ежегодно проходит лечение значительное число больных с лучевыми язвами конечностей и других областей тела, лучевыми повреждениями кишечника, мочевого пузыря и др. Основным компонентом местного лечения является препарат димексид (диметилсульфоксид, или ДМСО), применяющийся в виде перевязок раствора 5—10% или мази 10%. Это базовое лечение, назначаемое с учетом конкретных особенностей каждого больного, может дополняться назначением других антисептиков (диоксидин, хлоргексидин и др.), протеолитических ферментов, средств, стимулирующих репараторные процессы (куриозин, витаминизированные масла и др.). Разработанные схемы местного и общего лечения позволяют добиться благоприятных результатов у 57% пациентов [1, 2].
С сентября 2002 г. мы исследовали терапевтическую эффективность препарата гепон для лечения больных местными лучевыми повреждениями (см. таблицу 1).
 |
| Таблица 1. Применение гепона при лечении местных лучевых повреждений. |
Лучевые язвы у больных развились после лучевой терапии злокачественных опухолей (рак кожи — 16 пациентов, рак молочной железы — шесть, саркомы — четыре). Суммарная очаговая доза (СОД) составляла 45—70 Гр. Лучевые проктиты явились следствием лучевой терапии рака шейки и тела матки (13), рака мочевого пузыря (3) и прямой кишки (2). Лучевые циститы также наблюдались после лучевой терапии рака шейки и тела матки (13) и рака мочевого пузыря (4). Пневмофиброз — это следствие лучевой терапии лимфогранулематоза (6) и рака молочной железы (5 больных).
При лечении лучевых язв гепон применялся на первом этапе (7—10 дней) в виде орошения язвы раствором. Гепон (0,002) растворяли перед употреблением в 5 мл стерильного физиологического раствора. Орошение полученным раствором 0,04% гепона производилось ежедневно. На втором этапе, по мере развития грануляции, применялась мазь 0,04% (10—18 дней). Результаты лечения лучевых язв гепоном сопоставлялись с динамикой течения раневого процесса у более 800 больных, которым терапию проводили с принятыми в отделении методами лечения, состоящими в местном применении раствора 10% димексида (аппликации или электрофорез), электрофореза протеолитических ферментов и гепарина, использовании мазей левомиколя, ируксола, куриозина и эплана.
Эффективность применения гепона оценивалась клинически по состоянию раневой поверхности (уменьшение экссудации, скорости развития грануляций и скорости эпителизации язвы по Л. Н. Поповой (см. таблицу 2)), исчисляемой по формуле:
СЗ= (S-St)/St х 100, где
СЗ — скорость заживления
S — площадь лучевой язвы (мм 2 перед началом лечения)
St — площадь язвы (мм 2 ) в день измерения
t — время в сутках от начала лечения
 |
| Таблица 2. Скорость заживления лучевых язв. |
Положительный терапевтический эффект использования гепона мы склонны связывать в первую очередь с благоприятным его действием на микрофлору, что способствовало снижению воспалительного процесса и его негативных последствий (отек окружающих тканей, нарушение микроциркуляции и т. п.). Кроме того, важным аспектом действия гепона является его иммуномоделирующее действие, проявляющееся в активизации секреторного иммуноглобулина, снижении уровня противовоспалительных цитокинов, активизации a-интерферона, снижении адгезивной функции клеток и их апоптоза, прекращении вирусной репликации и повышении резистентности организма к бактериальной флоре.
В настоящее время, когда ранозаживляющее действие гепона доказано, лечение больных лучевыми язвами начинается с применения гепона, а затем дополняется, по показаниям, другими лекарственными средствами. Лечение лучевых ректитов (18 больных) и лучевых циститов (17 больных) проводилось в виде ежедневных двукратных микроклизм или инстилляций водного раствора 0,04% в течение 12—18 дней. Результаты применения гепона также сравнивались с результатами «традиционного» лечения, практиковавшегося в отделении в течение последних 25—30 лет (микроклизмы димексида 5—10%, эмульсии синтозона, витаминизированных масел и т. п.). Внутриполостное введение гепона уменьшало интенсивность болей и геморрагий и сокращало продолжительность лечения с 28—36 до 15—23 дней. Применение гепона активировало показатели иммунитета и у этой группы больных.
Таким образом, иммуномодулятор гепон в лечении больных с местными лучевыми повреждениями (лучевые язвы, лучевые ректиты и циститы) проявил себя как эффективное медикаментозное средство, способствующее быстрому снижению выраженности воспалительного процесса в поврежденных облучением тканях и ускорению репараторных процессов в них.
Литература
М. С. Бардычев, доктор медицинских наук, профессор
Медицинский радиологический научный центр РАМН (г. Обнинск)
Лучевой эпителиит что это
Лучевую терапию (ЛТ) обычно применяют для лечения рака шейки матки (РШМ) и злокачественных новообразований влагалища (иногда — диссеминированиого рака вульвы), а также в качестве адъювантной терапии у больных с высоким риском рака эндометрия (РЭ).
Индивидуальный подход к лучевой терапии (ЛТ) может быть применен практически при любых злокачественных новообразованиях женских половых органов, чтобы достичь временного облегчения. Осложнения после адекватной лучевой терапии (ЛТ) у больных раком шейки матки (РШМ) и раком влагалища обычно минимальны.
Однако, к сожалению, существует неправильное представление о частоте осложнений после лучевой терапии (ЛТ) как у медицинского персонала, так и у населения в целом. Можно предположить несколько источников происхождения такого мнения.
Во-первых, многие исследователи не понимают, что нежелательные побочные эффекты есть следствие неправильной техники терапии, и не должны экстраполировать их на адекватное использование методик лучевой терапии (ЛТ).
Во-вторых, осложнения лучевой терапии (ЛТ), как правило, отмечаются у неоперабельных больных с обширным опухолевым процессом.
Результаты лучевой терапии (ЛТ) в этих случаях не могут быть экстраполированы на применение оптимальных методик при местно-распространенных новообразованиях. Наконец, часто игнорируется тот факт, что большинство осложнений, приписываемых облучению, на самом деле есть результат неконтролируемого опухолевого процесса (например, прямокишечно-влагалищные и пузырно-влагалищные свищи).
Поскольку тонкая кишка, мочевой пузырь и прямая кишка примыкают к женским половым органам, большинство побочных эффектов и осложнений после лучевой терапии (ЛТ) связано с этими прилегающими органами. Осложнения, вызванные ЛТ, зависят от дозы, размера облучаемого поля и типа использованного оборудования. При неизменной дозе чем больше поле, тем больше риск осложнений. Как правило, при увеличении размера поля дозу снижают.
И наоборот, если поле уменьшается, можно использовать более высокую дозу. Применение брахитерапии также увеличивает риск местных осложнений. Наконец, по-видимому, использование комбинированной XT и ЛТ несколько увеличивает риск некоторых осложнений (например, нейтропении), но не приводит к серьезным отдаленным последствиям.
Осложнения, индуцированные лучевой терапией (ЛТ), можно разделить на острые и отсроченные. Осложнения лучевой терапии (ЛТ) вызываются ионизирующим и лучевым повреждением клеток, которые имеют митотическую активность, например желудочно-кишечный эпителий. Разрушение клеток слизистой оболочки приводит к ее истончению и обнажению, что сопровождается нарушением всасывания и потерей жидкости и электролитов (вследствие диареи).
Стволовые клетки слизистой оболочки ЖКТ, как правило, полностью восстанавливаются, и острые симптомы исчезают. Поздние осложнения могут быть вызваны различными механизмами тканевого нарушения, основанного на повреждении эндотелия. Облучение приводит к эндартерииту и постепенной закупорке мелких сосудов, последующая тканевая гипоксия — к фиброзу пораженных тканей.
Эти изменения прогрессируют и могут усугубляться в дальнейшем другими факторами поражения сосудов, такими как диабет, артериальная гипертензия и возрастные изменения сосудов. В тяжелых случаях можно обнаружить изъязвление, стриктуры, перфорацию и образование свищей.
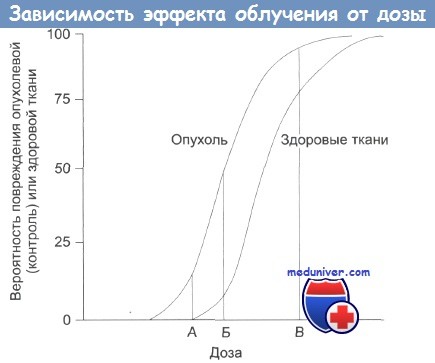
А — нижняя безопасная доза;
Б — увеличение дозы: растет поражение здоровых тканей;
В — наивысшая вероятность успешного лечения, но и высокая вероятность поражения здоровых тканей, многочисленные побочные эффекты, некоторые из которых могут проявиться в отдаленном будущем
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лучевой эпителиит что это
Текущий раздел: Обзоры
Низкоинтенсивное лазерное воздействие в программах реабилитации больных, получающих химиолучевое лечение (лекция)
Адрес документа для ссылки: h ttp://vestnik.rncrr.ru/vestnik/v11/papers/ shipil _ v 11. htm
Статья опубликована 30 ноября 2011 года.
Идентификационный номер статьи в ФГУП НТЦ “ИНФОРМРЕГИСТР”:
Сведения об авторах:
· Титова Вера Алексеевна, профессор, доктор медицинских наук, руководитель лаборатории радиохирургии и внутриполостных методов лечения, тел. +7(495) 333 9121, факс +7 (495) 334 7924
· Крейнина Юлия Михайловна, кандидат медицинских наук, старший научный сотрудник лаборатории радиохирургии и внутриполостных методов лечения, тел. +7(495) 333 9121
· Шевченко Людмила Николаевна, кандидат медицинских наук, научный сотрудник лаборатории радиохирургии и внутриполостных методов лечения, тел. +7(495) 333 9121,
· Петровский Владимир Юрьевич, кандидат медицинских наук, научный сотрудник лаборатории радиохирургии и внутриполостных методов лечения.
Эволюционные подходы к совершенствованию лазерных технологий (ЛТ) открыли новые возможности в лечении и реабилитации онкологических больных. Широкое внедрение вариантов химиолучевого лечения и применение методик сочетанной лучевой терапии злокачественных опухолей неизбежно сопряжено с ростом комбинированных осложнений. Понятным является стремление к поиску средств профилактики и консервативной коррекции последних на раннем периоде их возникновения. В Российском научном центре рентгенорадиологии был разработан и внедрен комплекс методов и средств коррекции местных и общих осложнений, одним из компонентов которого являлось воздействие низкоинтенсивным лазерным излучением, методика которого описана в этой лекции.
Ключевые слова: низкоинтенсивное лазерное излучение, надвенное перкутанное лазерное облучение крови, эпителиит, эпидермит, мукозит, гематологическая токсичность, рак шейки матки, рак вульвы, рак молочной железы, рак органов полости рта.
Low-intensity laser treatment in rehabilitation of patients treated with chemoradiotherapy
Эволюционные подходы к совершенствованию лазерных технологий (ЛТ) открыли новые возможности в лечении и реабилитации онкологических больных. Современные ЛТ подтвердили эффективность и целесообразность использования лазерного излучения для целей фотодинамической терапии, локальной гипертермии, а также – профилактики и лечения постхирургических воспалительных осложнений и осложнений химиолучевого лечения онкологических больных [1, 2].
В отделении радиохирургии ФГБУ РНЦРР Минздравсоцразвития совместно с ФГУП «Прибор» были проведены клинические исследования по разработке новых медицинских технологий и оценке эффективности применения универсального аппарата Лазон-ФТ, позволяющего в рамках последовательного применения выполнять фотодинамическую терапию, локальную гипертермию в качестве радиосенсебилизатора, и, как одного из важных компонентов интегрированного комплекса реабилитации больных, получающих интенсивную сочетанную лучевую терапию в сочетании с системной химиотерапией. Аппарат «Лазон-ФТ» имеет разрешение на бессрочное использование во всех медицинских учреждениях России.
Применение низкоинтенсивного лазерного излучения (НИЛИ) в онкологической практике до определенного времени было ограничено из-за возможного риска прогрессирования опухоли. Однако работы последних лет показали обоснованность использования НИЛИ для лечения и реабилитации больных со злокачественными новообразованиями. Многоплановые исследования академика Н.Д.Девяткова позволили сформулировать положение о возможности активного воздействия электромагнитных волн (ММ-волн) на биологические объекты, что обусловлено возникающими в плазматических мембранах биологических клеток акустоэлектрическими колебаниями. При этом появление этих биологических эффектов обусловлено, прежде всего, не энергетическим, а, скорее всего, «информационным» [3, 4, 5] воздействием низкоинтенсивных электромагнитных волн. По данным В.В.Файкина с соавт. за эффект торможения развития злокачественной опухоли под воздействием низкоэнергетического наноимпульсного ЭМИ ответственны два фактора:
· мобилизация защитных сил организма (повышение иммунитета) и
· непосредственное воздействие ЭМИ на сами злокачественные клетки [6].
Широкое внедрение вариантов химиолучевого лечения и применение методик сочетанной лучевой терапии злокачественных опухолей рака языка и дна рта, рака шейки и тела матки, вульвы, рака молочной железы неизбежно сопряжено с усилением многокомпонентного воздействия на высоко радиочувствительные ткани, окружающие опухоль. Это касается раннего развития эпителиитов, эпидермитов, энтеритов и других местных и системных осложнений, часто приводящих к нарушению режима облучения или введения цитостатиков и снижению их доз.
Показаниями к использованию НИЛИ являлись:
· реакции общей токсичности (астения, снижение аппетита, бессонница, снижение эмоционального фона, тошнота, рвота);
· гематологическая токсичность – лейкопения, анемия, тромбоцитопения I – III степени тяжести;
· наличие осложненных послеоперационных ран;
· местные осложнения – эпидермиты, мукозиты, эзофагиты, ларингиты разной степени тяжести.
Противопоказаниями к использованию терапии НИЛИ явились:
· полупроводниковые лазеры с диодной накачкой на длины волн 0,664 мкм и 1,06 мкм;
· комплект оптоволоконного инструмента (световоды) с различными по назначению насадками для оптимальной концентрации лазерного излучения в зависимости от клинической задачи;
· две пары очков со стеклами марки СЗС-22 для полной защиты глаза от силового излучения.
Методика проведения сеанса надвенной перкутанной терапии НИЛИ
Методика надвенной перкутанной терапии осуществлялась с использованием оптоволоконного инструмента (световода) с торцевым выводом излучения (рис.1). Для надвенной перкутанной терапии НИЛИ использовалось излучение с длиной волны 0,67 мкм, как наиболее эффективное для воздействия на кровь ввиду близости длины волны к максимуму поглощения крови, в режиме импульсного излучения с мощностью в импульсе 0,05-0,1 Вт. За 1 сеанс использовали 5–6 режимов лазерного излучения. Параметры воздействия задавались через встроенное в установку меню с указанием:
– вида воздействия (непрерывное или импульсное);
– параметров импульсов, их скважности и девиации, а также времени или числа импульсов воздействия. Параметры воздействия отображались на экране ЖКИ-установки.
Рис. 1. Сеанс надвенного перкутанного лазерного облучения крови на аппарате Лазон-ФТ.
Пациента усаживали, измеряли артериальное давление, пульс перед началом сеанса, и в области проекции кубитальной вены под контролем лазера-пилота (видимое излучение с мощностью до 3 мВт на длине волны 0,53 мкм, исходящее из того же волоконного инструмента и полностью пространственно совпадающее с рабочим) над местом облучения устанавливали световод. Аппарат включался для работы в заданном режиме (таблица 1). По истечении заданного времени рабочее лазерное излучение автоматическое отключалось. Использованы режимы, улучшающие микроциркуляцию, реологические свойства крови, стимулирующие гуморальный и клеточный иммунитет, лейко- и эритропоэз. В том случае, если во время сеанса пациент предъявлял жалобы на ухудшение самочувствия, головокружение, ощущение сердцебиения сеанс терапии НИЛИ прекращался, осуществляли контроль артериального давления, пульса и оказывали необходимую помощь. Время одного сеанса составляло 6-7мин., доза 15-20Дж за сеанс, количество сеансов в неделю до 3-5.
Таб. 1. Режимы, используемые для надвенной перкутанной терапии НИЛИ

