Метромикон или тержинан что лучше
Препараты против молочницы
Эта болезнь доставляет массу проблем, негативно влияет на образ жизни и отрицательно сказывается на сексуальной сфере. В данном материале вы узнаете, какие препараты существуют для лечения молочницы у женщин. В медицине она носит название вагинальный кандидоз.
Молочница у женщин
В течении жизни 3 из 4 женщин переносят хотя бы один случай вагинального кандидоза. Кроме этого, широкий спектр препаратов, существующих в свободной продаже, подталкивает к самолечению этой деликатной проблемы. Результатом этого стало учащение рецидивов и развитие устойчивости возбудителей к лекарственным препаратам.
Возбудитель молочницы условно-патогенный для организма, так как обитает в норме во влагалище, в ротовой полости, кишечнике. Когда баланс нарушается, происходит активный рост грибковой флоры и развитие воспалительной реакции на слизистых оболочках, так организм защищается от дальнейшего проникновения инфекции.
Факторы, нарушающие баланс :
У беременных также часто возникает эта проблема, так как меняется гормональный фон, снижается реактивность организма. Наличие молочницы может быть косвенным признаком инфекции передающейся половым путем.

Так как патоген может жить и размножаться внутри эпителиальных клеток слизистой оболочки, он имеет дополнительную защиту в виде мембраны самой клетки от действия лекарственных препаратов.
Виды болезни
Говорить о кандидоносительстве как об одном из видов болезни некоторые специалисты считают некорректным, так как данный род грибов присутствует и в нормальной флоре.
Симптомы
Симптомы при кандидозе достаточно характерные:
Проявления усиливаются после полового акта, водных процедур, согревания, во время сна, перед менструациями. При хроническом кандидозе проявления могут быть меньше, без большого количества выделений.
Лечение
Прежде чем бросаться в аптеку покупать препараты, нужно задуматься, что из факторов риска могло способствовать развитию молочницы и по возможности устранить их. Если это связано с лечением, назначенным доктором, не отменяйте его самостоятельно, обратитесь за консультацией к специалисту.
Препараты можно разделить на:
Местного действия – они практически не всасываются в общий кровоток, обладают минимальным количеством побочных эффектов, создают высокую концентрацию в зоне поражения. Эти особенности важны для беременных.
Но не всем комфортен путь введения препаратов. Также это может вызывать более быструю выработку резистентности к препарату и рецидиву симптомов. Возможны контактные дерматиты из-за состава средств.
Системного действия – в таблетированных формах. Эти средства часто имеют более короткий курс применения, воздействуют на очаги грибковой инфекции в других местах.
Несмотря на различия, механизм действия большинства препаратов заключается в нарушении процессов синтеза элементов клеточной стенки гриба.
Виды противокандидных препаратов
Полиеновые антибиотики
Нистатин, достаточно «древний» препарат и эффективность его сейчас не так велика. Леворин обладает общим токсическим действиям и противопоказан у беременных.
Группа имидазола
Это второе поколение антибиотиков обладает высокой эффективностью и низкой токсичностью. Выпускаются как для местного применения, так и в виде таблеток. Клотримазол для местного нанесения хорошо проникает в кожу и создает достаточные терапевтические концентрации. Низорал в виде таблеток хорошо всасывается в пищеварительном тракте и в достаточном количестве достигает очага инфекции. Но возможны реакции со стороны желудочно кишечного тракта, головокружения, может быть аллергическая реакция. Таблетированные формы противопоказаны при беременности, нарушении функции печени и почек. Ливарол (кетоконазол) в виде свечей. Курс длится 3-5 дней. Применение разрешено в период беременности и лактации, так как кетоконазол вводится местно.
Производные триазола
В основном используются для системного приема при лечении молочницы. Препараты флуконазола выводятся почками, в то время как итраконазол перерабатывается в печени и поэтому может оказывать влияние на обмен других лекарственных веществ.
Пиридоны
Батрафен, Дафнеджин (Циклопирокс Оламин). Наносятся в виде мази или 1% раствора не только во влагалище, но и обрабатываются пораженные участки кожи. В основном местное использование.
Комбинированные препараты
Благодаря комбинации антибиотиков между собой и с другими лекарственными веществами оказывают комплексный эффект при борьбе с грибком.
Другие
Нитрофунгин, декамин, препараты йода используются не так часто, так как имеют более низкую эффективность, по сравнению с представленными средствами.
Для выбора правильного препарата и устранения причин, приведших к молочнице, лучше обратиться к врачу. Это поможет снизить риск рецидивов и перехода в хроническую форму.
Результаты сравнительного исследования эффективности применения препаратов местного действия в терапии неспецифических воспалительных заболеваний влагалища
Опубликовано в журнале
«Российский вестник акушера-гинеколога», том 7, №3, 2007, стр.63-66
И.С. Сидорова, Е.И. Боровкова
Results of a comparative study of the efficacy of topical agents used in therapy for nonspecific vaginal inflammatory diseases
I.S. Sidorova, E.I. Borovkova
Кафедра акушерства и гинекологии факультета послевузовского профессионального образования (зав. — член-корр. РАМН проф. И.С. Сидорова) Московской медицинской академии им. И.М. Сеченова Обследованы 160 женщин репродуктивного возраста с бактериальным вагинозом с целью выбора наиболее эффективного способа медикаментозного лечения этого заболевания. В 4 группах по 40 человек каждая изучены лечебные эффекты тержинана (1-я группа), нео-пенотрана (2-я группа), далацина (3-я группа) и бетадина (4-я группа). Критериями эффективности лечения больных являлись исчезновение негативных субъективных проявлений клинических симптомов заболевания и нормализация лабораторных показателей. Установлено, что наибольший процент излечиваемости и минимальное число рецидивов наблюдались при применении тержинана и нео-пенотрана. Более предпочтительным является использование тержинана, так как он оказывает самое быстрое клиническое действие, положительно влияет на микроциркуляцию и слизистую оболочку влагалища и не дает системного эффекта.
A hundred and sixty reproductive-aged females with bacterial vaginosis were examined to select the most effective drug treatment for this disease. The therapeutic effects of terginan (Group 1), neo-penotran (Group 2), dalacin (Group 3), and betadine (Group 4) were studied, each group each comprising 40 females. The criteria for therapeutic efficiency were the disappearance of negative subjective manifestations of the disease and the normalization of laboratory indices. The highest cure rate and the minimum number of recurrences were observed in the use of terginan and neo-penotran. Terginan is the drug of choice as it exerts the rapidest clinical effect, and positively affects vaginal microcirculation and mucosa, and produces no systemic effect.
Проблема поиска оптимальных методов терапии инфекционной патологии в акушерстве и гинекологии является чрезвычайно актуальной, что связано с неуклонным ростом ее распространенности в популяции, появлением новых возбудителей, снижением чувствительности микроорганизмов к применяемым антибактериальным препаратам и доминированием в структуре возбудителей ассоциаций условно-патогенных микроорганизмов.
Бактериальный вагиноз (БВ) является одним из трех наиболее часто встречающихся инфекционных заболеваний нижнего отдела половой системы, составляя от 30 до 35%, наряду с вагинальным кандидозом (20-25%), и вагинитом, вызванным Trichomonas vaginalis (5-25%). У женщин репродуктивного возраста дисбактериоз влагалища встречается в 21-64% случаев, а у беременных этот показатель достигает 26%.
Дисбактериоз влагалища не сопровождается явлениями выраженного воспаления и лейкоцитарной реакции и развивается на фоне значительного подавления флоры молочно-кислых бактерий (палочка Дедерлейна) и факторов местного иммунитета. Он представляет собой клинический синдром, обусловленный патологическим изменением микробиоценоза влагалищной среды, что проявляется чрезмерно высокой концентрацией облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов и резким снижением или отсутствием молочно-кислых бактерий.
Применяемые в практике лекарственные средства должны обладать низкой токсичностью и высокой биодоступностью, низкой аллергенностью, достаточным спектром действия, минимальным количеством побочных эффектов, отсутствием тератогенного и эмбриотоксического действия на плод, а также приемлемой стоимостью. Однако не всегда предлагаемые препараты отвечают изложенным требованиям, а зачастую противоречат им. В арсенале акушера-гинеколога имеется достаточно широкий спектр лекарственных средств, применяя которые необходимо стремиться избегать полипрагмазии (использования нескольких препаратов одновременно), применять препараты с известным и обоснованно необходимым спектром действия, а при терапии моноинфекции использовать монокомпонентные препараты узкого спектра действия. В определенных ситуациях (во время беременности и лактации, при наличии экстрагенитальной патологии) необходимо отдавать предпочтение препаратам местного действия, не дающим системных эффектов.
В связи с регистрируемым неуклонным ростом распространенности инфекционной патологии, вызванной ассоциациями микроорганизмов, и прежде всего условно-патогенных, вызывающих неспецифические воспалительные заболевания, нами было проведено проспективное исследование, целью которого явилось изучение эффективности различных препаратов местного действия при дисбактериозе влагалища.
В качестве критериев оценки эффективности препаратов были выбраны:
Диагностика БВ в настоящее время не представляет трудностей. Нами использовался комплекс диагностических критериев, предложенный R. Amsel. и соавт. (1986):
Кроме того, мы проводили расширенное бактериологическое исследование — отделяемого на специфические дифференциально-диагностические среды. Материал из влагалища и шейки матки брали до проведения мануального исследования, после введения зеркал. Микробиологическое исследование проводилось 3-кратно: в момент поступления больной в клинику, через 3-4 дня после начала терапии и спустя 2 нед после прекращения антибактериальной терапии.
Посевы инкубировали в термостате при температуре 37°C в течение 24-96 ч в аэробных или анаэробных условиях в зависимости от исследуемой группы микроорганизмов. Анаэробиоз создавали в анаэростатах с помощью газогенерирующих пакетов емкостью 3,5 л. Идентификацию аэробных и анаэробных микроорганизмов осуществляли на основании изучения их морфологических и биохимических характеристик.
С помощью стереоскопического микроскопа подсчитывали число различных видов колоний в каждом секторе и рассчитывали количество lg КОЕ/мл.
Для БВ характерна общая массивная микробная обсемененность. Среди микроорганизмов преобладают морфотипы облигатных анаэробов и гарднереллы. Лактобациллы либо отсутствуют, либо число их исчисляется единицами (не более 5 в поле зрения). Поскольку заболевание не вызывается единственным микробным фактором, а имеет полимикробную природу в результате нарушения микробиоценоза влагалища и преобладания анаэробных микроорганизмов, при проведении корригирующей терапии возникает необходимость в применении препаратов, обладающих не только выраженной антианаэробной, но и противогрибковой активностью, а также не оказывающих выраженного влияния на активность нормальной микрофлоры и факторов местного иммунитета.
Целью лечения БВ является восстановление нормального микробиоценоза влагалища, терапия должна носить комплексный этиотропный и патогенетически обоснованный характер, а используемые препараты должны оказывать эффективное разнонаправленное действие.
Для достижения поставленной цели нами было проведено проспективное когортное исследование. Рабочую группу составили 160 женщин репродуктивного возраста (25±3 года) с подтвержденным диагнозом бактериального вагиноза. Бактериологическое исследование у пациенток проводилось в первую фазу менструального цикла, лечение начиналось после прекращения менструации.
Пациентки были рандомизированы на 4 группы по 40 человек (табл. 1.).
Таблица 1. Распределение пациенток по группам в зависимости от проводимого лечения
| Показатель | 1-я группа | 2-я группа | 3-я группа | 4-я групп |
|---|---|---|---|---|
| Используемый препарат | Тержинан | Нео-пенотран | Далацин | Бетади |
| Схемы применения | По 1 вагинальной таблетке на ночь в течение 10 дней | По 1 вагинальной свече на ночь в течение 10-14 дней | По 1 вагинальной свече на ночь в течение 6 дней | По 1 вагинальной свече на ночь в течение 14 дней |
Итак, 40 пациенток 1-й группы в качестве терапии бактериального вагиноза получали тержинан. Лечебный эффект этого комплексного препарата и его широконаправленный спектр действия обусловлен его составом:
Тержинан назначают интравагинально по 1 таблетке в течение 10 дней. Сочетание тернидазола и нистатина в данной ситуации очень выгодно, так как, во-первых, на фоне применения нитроимидазолов в 60% активируется кандидозная инфекция, во-вторых, преобладание в структуре инфекционных заболеваний бактериально-грибковых ассоциаций в настоящее время превышает 50%. Высокая эффективность тержинана обусловлена также входящим в его состав преднизолоном, который, не всасываясь в местный кровоток, нормализует микроциркуляцию в слизистых оболочек, способствуя притоку компонентов противовоспалительной защиты и оказывает регулирующее действие на факторы местного иммунитета и цитокины. Кроме всего перечисленного, происходит разжижение секрета и оптимизируется доставка антибактериальных препаратов к очагу воспаления.
Пациенткам 2-й группы был назначен нео-пенотран в виде вагинальных свечей. В состав препарата входит 500 мг метронидазола (достаточно высокая доза, при которой отмечается резорбтивное действие препарата) и 100 мг миконазола нитрат. Основная активность миконазола проявляется в отношении возбудителей дерматомикозов, разноцветного лишая, грамположительной флоры; он незначительно эффективен в отношении грибов рода Candida.
Женщины 3-й группы получали далацин в виде влагалищных свечей в течение 6 дней. В состав препарата входит 100 мг клиндамицина фосфата, представляющего собой полусинтетическое производное линкомицина и обладающее широким спектром активности в отношении целого ряда грамположительных и грамотрицательных анаэробных бактерий. Среди грамположительных анаэробов наибольшей чувствительностью к препарату обладают Peptococcus, Peptostreptococcus, Clostridium и др. Среди грамотрицательных анаэробов препарат эффективен в отношении Bacteroides, Fusobacterium и др.
Пациенткам 4-й группы был предложен бетадин в виде вагинальных свечей, содержащих 200 мг йодата поливинилпирролидона, в течение 14 дней (1 раз на ночь). Препарат активен в отношении многих бактерий, вирусов и грибов, однако оказывает в основном бактериостатическое действие. Использование препарата противопоказано при аллергии к йоду, гипертиреозе и во II и III триместрах беременности.
После назначения лечебных схем на 4-5-й день терапии у пациенток был взят материал из влагалища для проведения контрольного микробиологического исследования с целью оценки эффективности проводимой терапии (табл. 2). После окончания терапии через 14 дней проводилось контрольное исследование с целью установления излеченности и отсутствия рецидива заболевания. Критериями эффективности лечения больных с БВ являются исчезновение негативных субъективных проявлений клинических симптомов заболевания и нормализация лабораторных показателей.
Таблица 2. Результаты сравнительной оценки эффективности применяемых препаратов
| Препарат | Излечиваемость, % | Число рецидивов, % | Время наступления клинического улучшения | Время наступления микробиологического улучшения | Необходимость применения дополнительных средств |
|---|---|---|---|---|---|
| Тержинан | 98,0 | 2 | 1-й день | 3-й день | Нет |
| Нео-пенотран | 98,0 | 2 | 2-й день | 4-й день | Нет |
| Далацин | 97,0 | 3 | 3-й день | 3-й день | Антимикотик |
| Бетадин | 95,0 | 30 | 3-4-й день | 6-й день | Нет |
Итак, на фоне проводимого лечения наиболее эффективным оказались тержинан и нео-пенотран. Клиническое улучшение на фоне их применения отмечалось уже на 1-2-й день от начала лечения. На фоне развившегося воспалительного процесса увеличивается количество продуцируемого секрета, состоящего из отторгнутых эпителиальных клеток, транссудата, погибших микробных клеток, слизи. Все это обволакивает стенки влагалища, препятствуя проникновению лекарственных средств к воспаленному эпителию и замедляет достижение клинического улучшения. Кроме того, обязательным компонентом воспалительной реакции является первоначальная дилатация сосудов, сменяющаяся стойким спазмом сосудов, что, с одной стороны, препятствует распространению возбудителей из очага инфекции в кровоток, а с другой стороны, препятствует проникновению в очаг инфекции факторов противоинфекционной защиты (макрофагов, лейкоцитов). Поэтому, нормализация микроциркуляции является необходимым компонентом повышения эффективности проводимой терапии, что и было показано при применении тержинана.
Однако не всегда удается добиться быстрого клинического улучшения заболевания, а зачастую и излечения. По данным литературы, на фоне проводимой терапии в 20-60% случаев развивается рецидив бактериального вагиноза, что требует повторного проведения лечения. В нашей работе наибольшее число рецидивов заболевания развивались на фоне терапии бетадином (30%), что, видимо, связано с преобладанием бактериостатического действия препарата.
Необходимость в дополнительном назначении лекарственых средств возникала только при применении далацина, не имеющего в своем составе антимикотического компонента. Пациенткам 3-й группы дополнительно назначался дифлюкан в дозе 150 мг.
Итак, проведенное нами сравнительное исследование показало следующее:
Новое комбинированное топическое лекарственное средство для лечения хронического вульвовагинита
Опубликовано в журнале:
« Врач » сентябрь, 2015г. И. Сарвилина, доктор медицинских наук, Н. Кузьмина
Медицинский центр «Новомедицина», Ростов-на-Дону
Клиника «Скандинавия», Санкт-Петербург
Ключевые слова: хронический вульвовагинит, метронидазол, миконазол.
Самой частой причиной обращения пациенток к акушерам-гинекологам является вульвовагинальная инфекция. Удельный вес инфекционных вульвовагинитов (ВВГ) значительно увеличился, что связано с повышением качества лабораторной диагностики.
Наиболее распространены бактериальный вагиноз (до 50%), кандидозный ВВГ (20–25%), трихомонадный вагинит (15–20%) [3, 4]. Большую опасность представляют гонорейные и вирусные ВВГ в связи с хроническим рецидивирующим течением, вовлечением в процесс матки и ее придатков, развитием экстрагенитальных очагов инфекции и угрозы бесплодия [1].
Вульвовагинальная инфекция включает специфическую микрофлору (Trichomonas vaginalis, Treponema pallidum, Neisseria gonorrhoeae, Gardnerella vaginalis, Haemophilus ducreyi, Mycobacterium tuberculosis, Chlamydia trachomatis, различные вирусы), а также может развиваться вследствие дисбаланса нормальной микрофлоры, нарушаемой грибами, кишечной палочкой, другими энтеробактериями; β-гемолитическими стрептококками серогруппы В, энтерококками, анаэробами, урогенитальными микоплазмами. Бактериальные вагинозы связаны с выраженным ростом G. vaginalis, облигатных анаэробов, снижением числа влагалищных лактобактерий [6].
ВВГ часто рецидивирует. По данным международного исследования [4], включавшего 6000 женщин, распространенность кандидозного ВВГ составила 29–49%, рецидивы отмечались у каждой 5-й пациентки.
В проводимых исследованиях изучали возможности применения при вульвовагинальной инфекции ВВГ более высоких доз существующих лекарственных средств, а также осуществляется поиск новых комбинаций лекарственных веществ, путей их введения в организм и разработка улучшенных фармацевтических носителей активных веществ.
Лекарственные средства группы нитроимидазола являются синтетическими антимикробными препаратами с высокой активностью в отношении большинства облигатных грамположительных и грамотрицательных анаэробов, спорообразующих и неспорообразующих, включая анаэробные кокки; к чувствительны простейшие, Helicobacter pylori. По действию на анаэробные бактерии нитроимидазолы сопоставимы с клиндамицином, защищенными (3-лактамами, несколько уступают карбапенемам и некоторым фторхинолонам.
У микроорганизмов может вырабатываться устойчивость к нитроимидазолам в связи со снижением активности нитро-зоредуктаз микробной клетки и степени внутриклеточной трансформации лекарства, нарушением в работе транспортных систем клетки. Приобретенная резистентность микроорганизмов к нитроимидазолам может быть преодолена увеличением разовой дозы препарата при сохранении уровня безопасности и применением нового носителя активного нитроимидазола в лекарственной форме.
Рост расходов на медицинскую помощь пациенткам с ВВГ при ограниченных возможностях финансирования требует рационализации медицинских расходов при сохранении качества медицинской помощи. Отсутствует объективная сравнительная оценка препаратов по показателям фармакоэкономического анализа, на основе которой принимается решение об их включении в стандарты и протоколы ведения пациенток с ВВГ.
Исследование являлось пострегистрационным проспективным с параллельным дизайном и проводилось в соответствии с существующими в РФ правилами, а также принципами Декларации Хельсинки / Токио / Венеция / Гонконг / Вашингтон / Эдинбург / Сеул (1964–2008).
В исследование были включены 90 пациенток с диагнозом: хронический ВВГ, составившие с учетом схемы лечения 3 клинические группы; в контрольную группу вошли 20 пациенток с ВВГ, не получавшие терапию.
Критерии включения в исследование: амбулаторные больные в возрасте 18–45 лет; диагноз подострого и хронического ВВГ; отсутствие патологии печени, почек, нервной системы; соблюдение указаний врача; добровольное информированное согласие.
Критерии исключения из исследования: печеночная и почечная недостаточность; органические поражения центральной нервной системы (в том числе эпилепсия), лейкопения, беременность или кормление грудью; повышенная чувствительность или индивидуальная непереносимость компонентов препарата; психическое заболевание, активный туберкулез, алкоголизм и наркомания; злокачественное новообразование любой локализации; участие в другом клиническом исследовании в последние 3 мес; параллельное участие в другом аналогичном исследовании.
Клинико-анамнестическая характеристика пациентов включала оценку жалоб и анамнеза заболевания (длительность текущего рецидива, давность заболевания, средняя частота рецидивов ВВГ в год, длительность рецидива), результаты физикальных методов исследования, катамнестического наблюдения, данные о средней продолжительности межрецидивного периода, наличии сопутствующих заболеваний других органов и систем, сопутствующей терапии.
Применялись следующие методы исследования: общий анализ крови (анализаторы Advia 120 Bayer Diagnostics, Германия) и мочи (Clinitek Advantus, Siemens, США); рН-метрия вагинального секрета («Биосенсор АН», Россия); аминный тест; микроскопия; комплексное исследование вагинального секрета методом полимеразной цепной реакции – ПЦР (амплификатор «DT-96», Россия; детектор «Джин-4», Россия), культуральный и микологический методы, дискодиффузионный метод определения чувствительности для антибиотиков и антимикотических средств (по Keurby–Bauer); протеомный анализ вагинального секрета. Молекулярное фенотипирование вагинального секрета выполнялось в ходе центрифугирования (ацетон: HCl 10:1), фракционирования низкомолекулярных белков и пептидов (система MicroFlow MF10, Австралия) и идентификации белков и пептидов методом масс-спектрометрического анализа на основе MALDI-TOF-МС (прибор Autoflex III, Bruker, США). Применяли программное обеспечение для протеомики и масс-спектрометрии (Flex Control, Flex Analysis 2.x с функцией Auto Xecute, ClinProTools 1.0., Biotools 3.0.) и идентификацию пептидного фингерпринта молекулярных маркеров в интегрированной базе данных Mascot Search (v 2.1, Matrix Science, Великобритания).
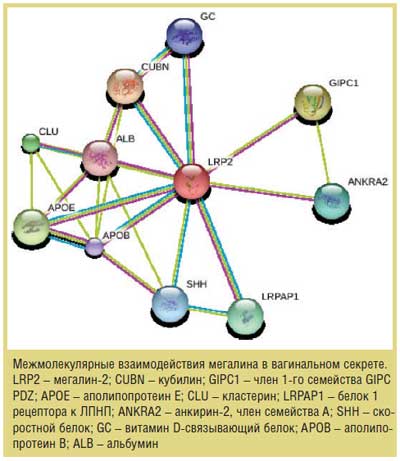
Результаты исследования представлены в виде молекулярного профиля вагинального секрета – пептиды и белки с указанием молекулярной массы (Mr) белков (Да). Условием для включения пептида и белка в диагностический профиль являлся показатель «покрытия сиквенса» при анализе масс-спектрограмм >15%. Биоинформационный анализ межмолекулярных взаимодействий пептидов и белков проведен на основе программы String 9.1.
Мониторинг безопасности терапии включал оценку частоты, характера, выраженности, длительности возникающих неблагоприятных побочных реакций и их связи с приемом препарата. Критериями эффективности терапии являлись оценка пациенткой течения заболевания: значительное улучшение – сокращение длительности рецидива и (или) увеличение длительности ремиссии в >2 раза; улучшение – сокращение длительности рецидива и (или) увеличение длительности ремиссии в Определение затрат на ведение больных предполагало оценку прямых затрат на лечение ВВГ, включавших затраты на 10-дневную терапию препаратами Метромикон-Неo ® (стоимость 1 упаковки – 316 руб.), Нео-Пенотран ® (стоимость 1 упаковки – 644 руб.), Тержинан ® (стоимость 1 упаковки – 492 руб.) и амбулаторное обслуживание (прием врача, осмотр, рН-метрия, аминотест, микроскопия, общий анализ крови и мочи, исследование флоры методами ПЦР, бактериологии и микологии; всего 6820 руб.) 2 раза за исследование, затраты на дополнительную диагностику и лечение в случае неэффективности терапии. Косвенные медицинские затраты пациентов были одинаковыми. Для определения затрат на медицинские услуги использовались тарифы на поликлинические медицинские услуги ТФОМС РО (2015) для пациенток с ВВГ. Для оценки затрат на лекарства использованы данные о ценах на лекарства Реестра лекарственных средств РФ. Выполнен анализ минимизации затрат при использовании препаратов-производных нитроимидазола и антимикотика у пациенток.
Расчеты соотношения затраты/ эффективность для каждого из вариантов лечения ВВГ проводили по формуле:
Кэ=C/Эф, где Кэ – коэффициент затратной эффективности, C – стоимость всех медицинских затрат при лечении конкретным препаратом; Эф – количественное выражение эффективности лекарств.
Статистическую обработку проводили c применением пакета программ Statistica 12.0.
При включении в исследование у всех участвующих в нем больных верифицировали диагноз ВВГ (на основе жалоб и анамнеза заболевания, физикального осмотра, характера влагалищного секрета, рН-метрии, аминного теста, микроскопии).
Клинико-анамнестическая характеристика пациентов контрольной и 3 исследуемых групп представлена в табл. 1.
Таблица 1.
Клинико-анамнестическая и лабораторная характеристика обследованных в сроки от 0 до 15-го дня (M±SD)
| Показатель | 1-я группа | 2-я группа | 3-я группа | Контроль |
|---|---|---|---|---|
| 0–15-й день | ||||
| Анамнестические данные* | ||||
| Возраст, годы | 34,8±2,5 | 34,5±2,3 | 34,7±2,4 | 34,5±2,3 |
| Масса тела, кг | 64,5±4,1 | 65,3±4,3 | 64,8±4,2 | 65,1±4,0 |
| Рост, см | 166,7±2,5 | 169,2±2,2 | 168,4±2,3 | 167,5±2,5 |
| Давность заболевания, годы | 3,7±1,0 | 3,6±0,9 | 3,8±1,0 | 3,6±0,8 |
| Средняя частота рецидивов ВВГ в год | 3,7+1,3 | 3,5±1,1 | 3,6±1,2 | 3,7+1,5 |
| Длительность рецидива ВВГ, дни | 11,0+1,5 | 10,5+1,3 | 12,2+1,6 | 11,5+1,7 |
| Средняя продолжительность межрецидивного периода, мес | 4,1±1,3 | 3,9±1,1 | 4,2±1,2 | 4,0±1,1 |
| рН-метрия, аминотест, микроскопия; день исследования | ||||||||
| 0-й | 15-й | 0-й | 15-й | 0-й | 15-й | 0-й | 15-й | |
| рН-метрия вагинального секрета рН>4,5, % | 100 | 0 | 100 | 3,3 | 100 | 10 | 100 | 100 |
| Положительный аминотест 10% КОН, % | 96,7 | 0 | 93,3 | 3,3 | 96,7 | 10 | 100 | 100 |
| Смешанная микрофлора, отсутствие лейкоцитов, наличие «ключевых клеток», % | 63,3 | 0 | 66,7 | 3,3 | 63,3 | 10 | 75 | 75 |
| Нормальная микрофлора, наличие бластопор и нитей мицелия, отсутствие «ключевых» клеток, % | 26,7 | 0 | 30 | 0 | 30 | 3,3 | 30 | 30 |
| Множество лейкоцитов, подвижные трихомонады (70%), отсутствие «ключевых» клеток, % | 16,7 | 0 | 13,3 | 0 | 16,7 | 0 | 15 | 15 |
| Примечание. * – Во всех случаях в разделе «Анамнестические данные» различия в 1–3-й группах по сравнению с контролем недостоверны. | ||||||||
Была выявлена высокая средняя частота рецидивов и большая их длительность при коротких межрецидивных периодах ВВГ (см. табл. 1).
До лечения (0-й день) были зарегистрированы клинические симптомы ВВГ: у большинства – наличие патологических белей, зуда вульвы, жжения (у всех), неприятного запаха (у 56,7% в 1-й, 60% – во 2-й, 3-й, контрольной группах), гиперемии и отечности слизистых (у всех), умеренного, гомогенного или негомогенного, белого, серого, пенистого, с запахом влагалищного секрета (у 56,7% – в 1-й и 3-й группах, 60% – во 2-й и контрольной группах), с творожистыми включениями (у 26,7% – в 1-й и 3-й группах, 33,3% – во 2-й группе, 30% – в контроле), реже выявляли болезненность при мочеиспускании (у 60% – в 1-й, 3-й и контрольной группах, 53,3% – во 2-й группе), диспареунию (у 50% – в 1-й группе, 40% – во 2-й, 3-й группах, 45% – в контроле), общее недомогание (у 36,7% – в 1-й и 3-й группах, 33,3% – во 2-й группе, 30% – в контроле), расчесы с изъязвлениями и гноевидным налетом (у 6,7% – в 1-й и 2-й группах, 3,3% – в 3-й группе, 5% – в контроле), бели желто-зеленого цвета (у 33,3% – в 1-й группе, 36,7% – во 2-й группе, 30% – в 3-й группе, 35% – в контроле), эндоцервицит и желтоватые гноевидные выделения на шейке матки (у 30% – в 1-й и 3-й группах, 36,7% – во 2-й группе, 35% – в контроле). У большинства пациенток обнаружены: pH>4,5, положительный аминотест, при микроскопии – смешанная микрофлора, отсутствие лейкоцитов, наличие «ключевых» клеток, часто в сочетании с бластопорами и нитями мицелия, у меньшего числа пациенток – множество лейкоцитов, подвижные трихомонады до 70%, отсутствие «ключевых» клеток (см. табл. 1).
В 0-й день у большинства пациенток выявляли умеренный дисбиоз, реже – выраженный. Данные бактериологического и микологического исследований показали рост Staphylococcus aureus, Enterococcus faecalis, Candida albicans в соскобе из влагалища и влагалищном секрете, реже – Escherichia coli, Proteus vulgaris, микоплазмы. Патогенные микроорганизмы были представлены Т. vaginalis (табл. 2).
Наибольшая чувствительность бактериальных возбудителей ВВГ отмечена к антибиотикам пенициллинового ряда с ингибиторами (3-лактамаз (76,7– 100%), цефалоспоринам и фторхинолонам (83,3–90,0%), С. albicans – к антимикотическим препаратам имидазолового (миконазол, итраконазол, кетоконазол) (100%) и триазолового ряда (флуконазол) (100%), за исключением клотримазола, чувствительность к которому была ниже при кандидозном или смешанном ВВГ (86,4%). Чувствительность Т. vaginalis оказалась наиболее высокой к производным нитроимидазола (100%), меньшей – к нифурателу (68,4%).
На 10-й день у пациенток 1-й группы отсутствовали симптомы ВВГ, а также его проявления при физикальном осмотре, по данным рН-метрии, аминотеста, микроскопии. У пациенток 2-й и 3-й групп на 10-й день выявлены патологические бели, зуд вульвы и жжение, гиперемия слизистых оболочек, умеренные, гомогенные, белые/серые, пенистые с запахом выделения, pH>4,5, положительный аминотест, при микроскопии – смешанная микрофлора, отсутствие лейкоцитов, наличие «ключевых» клеток (частота каждого признака: 3,3% во 2-й и 10% – в 3-й группе). В 3-й группе на 10-й день сохранялись болезненность при мочеиспускании (6,7%), гиперемия и отек слизистой влагалища (10%), негомогенные выделения с творожистыми включениями и наличие бластоспор и нитей мицелия во влагалищном секрете (3,3%).
На 10-й день показано уменьшение доли пациенток с умеренным дисбиозом влагалища во всех исследуемых группах по сравнению с контролем при отсутствии пациенток с выраженным дисбиозом влагалища в 1-й группе и наличии их во 2-й и 3-й группах. При этом нормоценоз влагалища на фоне применения препарата Метромикон-Неo ® регистрировался чаще, чем при использовании препаратов Нео-Пенотран ® и Тержинан ® (см. табл. 2).
Таблица 2.
Динамика показателей ПЦР, бактериологического и микологического исследования вагинального секрета при ВВГ
Динамика молекулярных иммуновоспалительных процессов в вагинальном секрете, определяющих механизм эффективности топической формы метронидазола и миконазола при ВВГ, представлена в табл. 3: на фоне использования суппозиториев Метромикон-Неo ® зарегистрировано наиболее значительное уменьшение числа пациенток с высокой экспрессией (3-амилоида 42, белка F, ренина, транскрипционного фактора SP1, мегалина, субъединицы В тромбоцитарного фактора роста и увеличение – с высокой экспрессией фактора C1q-комплемента и молекулы 3, ингибирующей Fas-опосредованный апоптоз в вагинальном секрете по сравнению с контролем; во 2-й и 3-й группах динамика экспрессии маркеров иммуновоспалительных процессов в вагинальном секрете была менее выраженной.
Таблица 3.
Динамка протеомного профиля вагинального секрета у пациенток с ВВГ; %
| Белок | Mr, Да | 1-я группа | 2-я группа | 3-я группа | Контроль | ||||
|---|---|---|---|---|---|---|---|---|---|
| День исследования | |||||||||
| 0-й | 15-й | 0-й | 15-й | 0-й | 15-й | 0-й | 15-й | ||
| β-амилоид | 4286 | 943 | 100 | 83,3 | 100 | 93,3 | 100 93,3 | 100 | 100 |
| Фактор C1q-комплемента | 26 017 | 70 | 96,7 | 73,3 | 83,3 | 73,3 | 80 | 85 | 85 |
| Молекула 3, ингибирующая Fas-опосредованный апоптоз | 43 146 | 76,7 | 93,3 | 80 | 96,7 | 80 | 93,3 | 85 | 85 |
| Белок F | 32 586 | 100 | 73,3 | 100 | 76,7 | 100 | 80 | 80 | 80 |
| Ренин | 45 057 | 96,7 | 66,7 | 96,7 | 80 | 93,3 | 80 | 90 | 90 |
| Транскрипционный фактор SP1 | 80 693 | 93,3 | 63,3 | 93,3 | 80 | 96,7 | 76,7 | 80 | 80 |
| Мегалин | 530 166 | 100 | 63,3 | 96,7 | 83,3 | 100 | 93,3 | 90 | 90 |
| β-Субъединица тромбоцитарного фактора роста | 27 283 | 40 | 96,7 | 53,3 | 100 | 60 | 96,7 | 95 | 95 |
| Примечание. % – доля пациенток с экспрессией белка/пептида. | |||||||||
Таблица 4.
Динамика показателей КЖ по опроснику SF-36 Health status survey у обследованных (M±SD); баллы
Зарегистрированы неблагоприятные побочные реакции при применении топической формы тернидазола и нистатина в препарате Тержинан ® (чувство жжения и раздражение слизистой оболочки – у 2 пациенток), верифицированные как легкая степень тяжести.
Лечение пациенток с ВВГ препаратом Метромикон-Неo ® в течение 10 дней оказалось наиболее эффективным: значительное улучшение состояния здоровья и отсутствие рецидива ВВГ в ближайшие 3 мес отметили все пациентки 1-й группы; 26 (86,7%) женщин 2-й группы и 20 (66,7%) – 3-й.
Суммарные прямые затраты на 10-дневную терапию ВВГ представлены в табл. 5: стоимость амбулаторного ведения пациенток во 2-й и 3-й группах оказалась выше, чем в 1-й. Наибольшая эффективность и наименьший коэффициент затратной эффективности показаны для терапии ВВГ для Метромикон-Неo ® по сравнению с терапией препаратами Нео-Пенотран ® и Тержинан ® (см. табл. 5).
Таблица 5.
Фармакоэкономический анализ при использовании топических форм нитроимидазола и антимикотиков у пациенток с ВВГ