Миндалины мозжечка выше уровня чемберлена что означает
Миндалины мозжечка выше уровня чемберлена что означает
1. Общие характеристики мальформации Арнольда-Киари I типа:
• Лучшие диагностические критерии:
о Комбинация опущения «заостренных» миндалин мозжечка с «тесной» задней черепной ямкой, сужающей ретроцеребеллярные ликворные пространства на уровне большого затылочного отверстия/верхнего шейного отдела позвоночника
• Морфология:
о Низколежащие заостренные миндалины мозжечка конической формы с косой вертикальной бороздой, удлиненный, но нормально расположенный IV желудочек (нормальный дорсально направленный шатер)
2. КТ при мальформации Арнольда-Киари I типа:
• КТ, костное окно:
о Обычно без изменений; в атипичных случаях => короткий скат, сегментация/аномалии соединения костных структур КВП
3. МРТ при мальформации Арнольда-Киари I типа:
• Т1-ВИ:
о Заостренные (не закругленные) миндалины мозжечка, расположенные на 5 и более мм ниже большого затылочного отверстия о «Тесное» большое затылочное отверстие с уменьшенными/отсутствующими цистернами
о ± удлинение IV желудочка, аномалии заднего мозга
• Т2-ВИ:
о Косые листы миндалин мозжечка (похожие на лычки сержанта)
о ± короткий скат => видимое опущение IV желудочка, продолговатого мозга
о ± сирингомиелия (14-75%)
• Кино-МРТ:
о Беспорядочная пульсация ЦОК, Т подвижности ствола мозга/ миндалин мозжечка => Т пиковой систолической скорости, снижение тока ЦСЖ через большое затылочное отверстие
— Пульсация миндалин мозжечка может быть более информативным показателем по сравнению с током ЦСЖ
4. Рекомендации по визуализации мальформации Арнольда-Киари I типа:
• Лучший инструмент визуализации:
о Мультипланарная МРТ + сагиттальная кино-МРТ
в) Дифференциальная диагностика мальформации Арнольда-Киари I типа:
1. Смещение миндалин мозжечка ниже большого затылочного отверстия как вариант нормы:
• Миндалины в норме могут лежать ниже большого затылочного отверстия
• Мальформация Арнольда-Киари I типа маловероятна, кроме случаев, когда миндалины заострены и обтурируют БЗО
г) Патология мальформации Арнольда-Киари I типа:
г) Клиническая картина мальформации Арнольда-Киари I типа:
3. Течение и прогноз:
• Естественное течение до конца не изучено:
о У многих пациентов отсутствуют клинические проявления, мальформация Арнольда-Киари I типа выявляется случайно
о Чем выраженнее эктопия =>, тем выше риск сирингомиелии
• Ответ на лечение выше у детей, чем у взрослых
д) Диагностическая памятка:
1. Обратите внимание:
• Степень опущения миндалин мозжечка коррелирует с тяжестью клинического течения
• Клинически значимы, вероятно, только случаи с опущением миндалин > 5 мм и их заострением ± «тесная» задняя черепная ямка»
2. Советы по интерпретации исследований:
• Не используйте критерий 5 мм изолированно для диагностики мальформации Арнольда-Киари I типа (учитывайте и другие признаки, клинические проявления)
е) Список литературы:
Редактор: Искандер Милевски. Дата публикации: 24.2.2019
Аномалия Арнольда-Киари
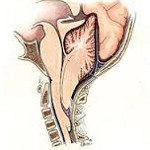
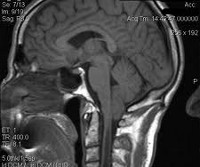
Аномалия Арнольда-Киари – это врожденная патология развития ромбовидного мозга, проявляющаяся несоответствием размеров задней черепной ямки и мозговых структур находящихся в этой области, что приводит к опущению ствола головного мозга и миндалин мозжечка в большое затылочное отверстие и ущемлению их на этом уровне.
Частота этого заболевания составляет от 3.3 до 8.2 наблюдений на 100000 населения.
Патогенез (что происходит?) во время Аномалии Арнольда-Киари :
Анатомические особенности аномалии Киари
Мозжечок расположен в задней черепной ямке.
На уровне большое затылочного отверстия нижний отдел ствола мозга (продолговатый мозг) переходит в спинной мозг. В норме спино-мозговая жидкость (ликвор) свободно циркулирует в субарахноидальных пространствах головного и спинного мозга. На уровне большого затылочного отверстия субарахноидальные пространства головного и спинного мозга соединяются, что обеспечивает свободный отток ликвора от головного мозга.
При аномалии Киари низко расположенные миндалины мозжечка затрудняют свободную циркуляцию спиномозговой жидкости между головным и спинным мозгом. Миндалины блокируют большое затылочное отверстие, как пробка затыкает бутылочное горлышко. В результате нарушается отток ликвора и развивается гидроцефалия.
Симптомы Аномалии Арнольда-Киари :
Аномалии III и IV типов обычно несовместимы с жизнью.
Примерно у 80% пациентов аномалия Арнольда-Киари сочетается с патологией спинного мозга – сирингомиелией, которая характеризуется образованием в спинном мозге кист, вызывающих прогрессирующую миелопатию. Эти кисты образуются при опущении структур задней черепной ямки и сдавление шейного отдела спинного мозга.
Типичная клиническая картина аномалии Арнольда-Киари характеризуется следующими симптомами:
— боль в шейно-затылочной области усиливающаяся при кашле, чихании,
— снижение болевой и температурной чувствительности в верхних конечностях,
— снижение мышечной силы в верхних конечностях,
— спастичность верхних и нижних конечностей,
— обмороки, головокружения,
— снижение остроты зрения,
— в более запущенных случаях присоединяются: эпизоды апноэ (короткая остановка дыхания), ослабление глоточного рефлекса, непроизвольные быстрые движения глаз.
Диагностика Аномалии Арнольда-Киари :
Иногда аномалия Киари никак не проявляет себя и выявляется случайно при диагностических процедурах.
В настоящий момент методом выбора при диагностике данной патологии является МРТ головного мозга шейного и грудного отделов спинного мозга (для исключения сирингомиелии).
Лечение Аномалии Арнольда-Киари :
Если единственным симптомом заболевания является незначительной интенсивности болевой синдром, для лечения применяется консервативная терапия, которая включает в себя различные схемы с примененим нестероидных противовоспалительных препаратов и миорелаксантов.
При отсутствии эффекта от консервативной терапии в течение 2-3 месяцев или наличии у пациента неврологического дефицита (онемение, слабость а конечностях и т.д.) показано проведение операции.
Целью операции является устранение сдавления нервных структур и нормализация тока цереброспинальной жидкости, для чего производится увеличение объема задней черепной ямки. В результате лечения, как правило, уменьшается, или исчезает головная боль, частично восстанавливаются чувствительность и двигательные функции.
К каким докторам следует обращаться если у Вас Аномалия Арнольда-Киари :
Синдром Арнольда — Киар
Педиатр Анна Колинько о патологии развития головного мозга, которая может встречаться у 30 % населения
Синдром хронической усталости, головокружения и боль в шее могут быть следствием мальформации (аномалии) Арнольда — Киари. После начала широкого использования МРТ стало понятно, что болезнь встречается у 14–30 % популяции
Все первые описания мальформации были посмертными. В 1883 году шотландский анатом Джон Клеланд (J. Cleland, 1835–1925 гг.) впервые описал удлинение ствола и опущение миндалин мозжечка в большое затылочное отверстие у 9 умерших новорожденных. В 1891 году австрийский патолог Ганс фон Киари (H. Chiari, 1851–1916 гг.) подробно охарактеризовал 3 типа мальформации у детей и взрослых. А в 1894 году немецкий патолог Юлиус Арнольд (J. Аrnold, 1835–1915 гг.) подробно описал синдром Киари 2 типа, в сочетании со спинномозговой грыжей (spina bifida). В 1896 году Киари дополнил свою классификацию четвертым типом. В 1907 году ученики Арнольда использовали термин «мальформация Арнольда — Киари» по отношению к аномалии 2 типа. Теперь это название распространилось на все типы. Некоторые врачи справедливо отмечают, что вклад Арнольда несколько преувеличен и верным будет термин «мальформация Киари».
Версии о причинах
Этиология и патогенез синдрома Арнольда — Киари остаются неуточненными. Киари предположил, что смещение мозжечка и продолговатого мозга происходит из‑за внутриэмбриональной гидроцефалии, которая возникает как следствие стеноза сильвиева водопровода — узкого канала длиной 2 см, который соединяет III и IV желудочки мозга.
Типы мальформаций
1 тип — опущение миндалин мозжечка в позвоночный канал ниже уровня большого затылочного отверстия с отсутствием спинномозговой грыжи. У 15–20 % пациентов этот тип сочетается с гидроцефалией, а у 50 % больных — с сирингомиелией — заболеванием, при котором в спинном и продолговатом мозге образуются полости. В 1991 году было предложено подразделить аномалии Арнольда — Киари 1 типа на тип А — с сирингомиелией и тип В — без сирингомиелии.
Сирингомиелии при Арнольде — Киари 1 степени.
Энцефаломенингоцеле — врожденная грыжа головного мозга и его оболочек, содержащая цереброспинальную жидкость.
Спинальная дизрафия — порок развития, заключающийся в отсутствии слияния по средней линии парных закладок кожи, мускулатуры, позвонков, спинного мозга
2 тип — опущение нижних отделов червя мозжечка, продолговатого мозга и IV желудочка. Отличительным признаком данного типа является сочетание со спинномозговой грыжей (spina bifida) в поясничном отделе, отмечается прогрессирующая гидроцефалия, часто — стеноз водопровода мозга. Среди детей с менингомиелоцеле до 90 % случаев сопровождается аномалией Арнольда — Киари 2 степени.
0, 1 и 2 степени синдрома Арнольда — Киари наиболее распространены в популяции. III и IV типы обычно несовместимы с жизнью.
Симптоматика
Терапия
Лечение аномалий Арнольда — Киари зависит от выраженности неврологической симптоматики. Консервативная терапия включает в себя нестероидные противовоспалительные препараты и миорелаксанты. Если в течение 2–3 месяцев консервативная терапия безрезультатна или у пациента имеется выраженный неврологический дефицит, показано оперативное вмешательство. В процессе операции устраняется сдавление нервных структур и нормализуется ликвороток путем увеличения объема (декомпрессии) задней черепной ямки и установки шунта. Оперативное лечение эффективно, по разным источникам, в 50–85 % случаев, в оставшихся случаях симптоматика регрессирует не полностью. Операцию рекомендуется выполнять до развития тяжелого неврологического дефицита, поскольку восстановление происходит лучше при минимальных изменениях неврологического статуса. Подобное оперативное лечение выполняется почти в каждом федеральном нейрохирургическом центре России и проводится в рамках высокотехнологичной медицинской помощи по системе ОМС.
Аномалия Киари ( Синдром Арнольда-Киари )
Аномалия Киари (синдром Арнольда-Киари) — заболевание, при котором структуры головного мозга, расположенные в задней черепной ямке, опущены в каудальном направлении и выходят через большое затылочное отверстие. В зависимости от типа аномалия Киари может проявляться головной болью в затылке, болью в шейном отделе, головокружением, нистагмом, обмороками, дизартрией, мозжечковой атаксией, парезом гортани, снижением слуха и ушным шумом, нарушением зрения, дисфагией, дыхательными апноэ, стридором, расстройствами чувствительности, гипотрофией мышц и тетрапарезом. Аномалия Киари диагностируется путем проведения МРТ головного мозга, шейного и грудного отделов позвоночника. Аномалия Киари, сопровождающаяся стойким болевым синдромом или неврологическим дефицитом, подлежит хирургическому лечению (декомпрессия задней черепной ямки или шунтирующие операции).
МКБ-10
Общие сведения
Аномалия Киари встречается по различным данным у 3-8 человек на 100 тысяч населения. В зависимости от типа аномалия Киари может диагностироваться в первые дни после рождения ребенка или стать неожиданной находкой у взрослого пациента. В 80% случаев аномалия Киари сочетается с сирингомиелией.
Причины
До сих пор аномалия Киари остается заболеванием, об этиологии которого в неврологии нет единого мнения. Ряд авторов считает, что аномалия Киари связана с уменьшенным размером задней черепной ямки, приводящим к тому, что по мере роста расположенных в ней структур они начинают выходить через затылочное отверстие. Другие исследователи предполагают, что аномалия Киари развивается в результате увеличенных размеров головного мозга, который при этом как бы выталкивает содержимое задней черепной ямки через затылочное отверстие.
Спровоцировать переход незначительно выраженной аномалии в выраженную клиническую форму может гидроцефалия, при которой за счет увеличения желудочков увеличивается общий объем мозга. Поскольку аномалия Киари наряду с дисплазией костных структур краниовертебрального перехода сопровождается недоразвитием связочного аппарата этой области, любая черепно-мозговая травма может приводить к усугублению вклинения миндалин мозжечка в затылочное отверстие с манифестацией клинической картины заболевания.
Классификация
Аномалия Киари подразделяется на 4 типа:
Аномалия Киари II и Киари III часто наблюдается в комбинации с другими дисплазиями нервной системы: гетеротопией коры головного мозга, полимикрогирией, аномалиями мозолистого тела, кистами отверстия Можанди, перегибом сильвиевого водопровода, гипоплазией подкорковых структур, намета и серпа мозжечка.
Симптомы аномалии Киари
Наиболее часто в клинической практике встречается аномалия Киари I типа. Она проявляется ликворногипертензионным, церебеллобульбарным и сирингомиелическим синдромами, а также поражением черепно-мозговых нервов. Обычно аномалия Киари I манифестирует в период полового созревания или уже во взрослом возрасте.
Для ликворногипертензионного синдрома, которым сопровождается аномалия Киари I, характерна головная боль в затылке и шейной области, усиливающаяся во время чихания, кашля, натуживания или напряжения мышц шеи. Может наблюдаться рвота, не зависящая от приема пищи и ее характера. При осмотре пациентов с аномалией Киари выявляется повышенный тонус мышц шеи. Среди мозжечковых нарушений наблюдаются нарушение речи (дизартрия), нистагм, мозжечковая атаксия.
Поражение ствола мозга, расположенных в нем ядер черепно-мозговых нервов и их корешков проявляются снижением остроты зрения, диплопией, расстройством глотания, снижением слуха по типу кохлеарного неврита, системным головокружением с иллюзией вращения окружающих предметов, ушным шумом, синдромом сонных апноэ, повторяющимися кратковременными потерями сознания, ортостатическим коллапсом. Пациенты, у которых имеется аномалия Киари, отмечают усиление головокружения и ушного шума при поворотах головой. Поворот головы у таких больных может спровоцировать обморок. Может отмечаться атрофические изменения половины языка и парез гортани, сопровождающийся осиплостью голоса и затруднением дыхания. Возможен тетрапарез с большим снижением мышечной силы в верхних конечностях, чем в нижних.
В случаях, когда аномалия Киари I сочетается с сирингомиелией, наблюдается сирингомиелический синдром: нарушения чувствительности по диссоциированному типу, онемения, мышечные гипотрофии, тазовые нарушения, нейроартропатии, исчезновение брюшных рефлексов. При этом некоторые авторы указывают на несоответствие размера и местонахождения сирингомиелической кисты распространенности расстройств чувствительности, степени выраженности парезов и мышечной гипотрофии.
Аномалия Киари II и Киари III имеют сходные клинические проявления, которые становятся заметны с первых минут жизни ребенка. Аномалия Киари II сопровождается шумным дыханием (врожденный стридор), периодами кратковременной остановки дыхания, двусторонним нейропатическим парезом гортани, нарушением глотания с забросом жидкой пищи в нос. У новорожденных аномалия Киари II проявляется также нистагмом, повышением мышечного тонуса в верхних конечностях, цианозом кожных покровов, возникающим во время кормления. Двигательные расстройства могут быть выражены в различной степени и прогрессировать вплоть до тетраплегии. Аномалия Киари III имеет более тяжелое течение и зачастую является не совместимым с жизнью нарушением развития плода.
Диагностика
Неврологический осмотр и стандартный перечень неврологических обследований (ЭЭГ, Эхо-ЭГ, РЭГ) не дают специфических данных, позволяющих установить диагноз «аномалия Киари». Как правило, они выявляют лишь признаки значительного повышения внутричерепного давления, т. е. гидроцефалию. Рентгенография черепа выявляет только костные аномалии, которыми может сопровождаться аномалия Киари. Поэтому до внедрения в неврологическую практику томографических методов исследования диагностика этого заболевания представляла для невролога большие затруднения. Теперь врачи имеют возможность поставить таким пациентам точный диагноз.
Следует отметить, что МСКТ и КТ головного мозга при хорошей визуализации костных структур краниовертебрального перехода не позволяют достаточно точно судить о мягкотканных образованиях задней черепной ямки. Поэтому единственным достоверным методом диагностики аномалии Киари на сегодняшний день является магнитно-резонансная томография. Ее проведение требует обездвиженности пациента, поэтому у маленьких детей она проводится в состоянии медикаментозного сна. Кроме МРТ головного мозга для выявления менингоцеле и сирингомиелических кист необходимо также проведение МРТ позвоночника, особенно его шейного и грудного отделов. При этом проведение МРТ исследований должно быть направлено не только на диагностику аномалии Киари, но и на поиск других аномалий развития нервной системы, которые часто с ней сочетаются.
Лечение аномалии Киари
Бессимптомно протекающая аномалия Киари не нуждается в лечении. В случаях, когда аномалия Киари проявляется лишь наличием болей в шее и затылочной области, проводят консервативную терапию, включающую анальгетические, противовоспалительные и миорелаксирующие препараты. Если аномалия Киари сопровождается неврологическими нарушениями (парезы, расстройства чувствительности и мышечного тонуса, нарушения со стороны черепно-мозговых нервов и пр.) или не поддающимся консервативной терапии болевым синдромом, то показано ее хирургическое лечение.
Наиболее часто в лечении аномалии Киари применяется краниовертебральная декомпрессия. Операция включает расширение затылочного отверстия за счет удаления части затылочной кости; ликвидацию сдавления ствола и спинного мозга за счет резекции миндалин мозжечка и задних половин двух первых шейных позвонков; нормализацию циркуляции цереброспинальной жидкости путем подшивания в твердую мозговую оболочку заплаты из искусственных материалов или аллотрансплантата. В некоторых случаях аномалия Киари лечится при помощи шунтирующих операций, направленных на дренирование цереброспинальной жидкости из расширенного центрального канала спинного мозга. Цереброспинальная жидкость может отводиться в грудную или брюшную полость (люмбоперитонеальное дренирование).
Прогноз
Важное прогностическое значение имеет тип, к которому относится аномалия Киари. В некоторых случаях аномалия Киари I может на протяжении всей жизни пациента сохранять бессимптомное течение. Аномалия Киари III в большинстве случаев приводит к летальному исходу. При появлении неврологических симптомов аномалии Киари I, а также при аномалии Киари II большое значение имеет своевременное проведение хирургического лечения, поскольку возникший неврологический дефицит плохо восстанавливается даже после успешно проведенной операции. По различным данным эффективность хирургической краниовертебральной декомпрессии составляет 50-85%.
Вертеброгенное головокружение: клиника, диагностика, лечение
Н. А. Дайхес, О. В. Зайцева ФГУ НКЦ оториноларингологии Росздрава (директор – д. м. н., профессор Дайхес Н. А.)
Головокружение в последние годы становится все более частым симптомом, встречающимся в медицинской практике. Головокружением страдают 3 – 4% пациентов, обращающихся к врачам-интернистам и 10% больных, посещающих оториноларингологов и невропатологов (26). Причиной головокружения могут являться более 80 патологических состояний (23).
Одной из основных причин развития вестибулярных расстройств у лиц трудоспособного возраста являются остеохондроз шейного отдела позвоночника и вертебробазилярная дисциркуляция (1, 5, 18). У 49,6% больных шейным остеохондрозом выявляются вестибулярные нарушения (обследовано 113 человек) (6). До 82% пациентов, страдающих шейным остеохондрозом, еще задолго до первого приступа головокружения жалуются на неустойчивость при ходьбе, ощущение зыбкости почвы под ногами, неопределенное покачивание тела, неясность контуров предметов.
Вегетативные нарушения, включающие вестибуло-вегетативно-сосудистый синдром, встречаются у 47% больных шейным остеохондрозом (5), что во многом определяет клиническую картину: вазомоторные вегетативно-ирритативные проявления (ушной шум, головокружение, тошнота, синкопальные приступы), а также «неврологический дефицит». Вестибулярные нарушения составляют одно из наиболее ярких проявлений синдрома позвоночной артерии (задний шейный симпатический синдром или синдром Барре – Льеу), который в 30 – 42,5% случаев может быть обусловлен остеохондрозом или аномальным строением шейного отдела позвоночника, вызываться унковертебральными экзостозами (6) и разгибательным подвывихом позвонков (25), образуя блоки (полное или частичное слияние тел позвонков, дужек, суставных или остистых отростков соседних позвонков, что может быть связано с нарушением сегментации во внутриутробном периоде), чаще на уровне СII – СIII (16). При мануальном исследовании шейного отдела позвоночника 82 больных нейросенсорной тугоухостью, лечение которых по общепринятым схемам не было эффективным, у всех выявлены ротационные блоки в сторону больного уха преимущественно в нижне- и среднешейных позвоночных двигательных сегментах, у 69 человек – блоки в атланто-затылочном сочленении с больной стороны (19). Головокружение при синдроме позвоночной артерии может быть как несистемным – в виде покачивания, дурноты, так и системным – в виде вращения предметов, ощущения «ухода почвы из-под ног». Иногда встречается сочетание системного и несистемного головокружения.
Дегенеративные изменения связочно-хрящевых и костных структур шейного отдела позвоночника приводят к раздражению, а иногда и к сдавливанию, оплетающего позвоночную артерию симпатического нервного сплетения, которое оказывает влияние на сосудистую систему и метаболизм внутреннего уха. (4). Раздражение позвоночного нерва, повышая тонус позвоночной артерии, может уменьшить скорость объемного кровотока в ней на треть от исходной величины, при этом усиливается тонус и в ветвях основной артерии, в частности снижается более чем на 40% кровоснабжение внутреннего уха. Длительное патологическое воздействие на шейное симпатическое сплетение может вызвать сосудистые расстройства в лабиринте и нарушение функции рецепторного аппарата внутреннего уха (14).
Дегенеративно-дистрофические изменения, развивающихся в шейном отделе позвоночника, могут вызвать такое осложнение как стеноз позвоночного канала, проявляющийся признаками поражения нервной системы. Причиной стеноза нередко являются межпозвонковые грыжи, чаще сегментов С5 – С6 и С6 – С7, полисегментарное поражение встречается в 82% случаев (7).
При изучении состояния двигательных сегментов позвоночника (методом компьютерной томографии) на ранних стадиях процесса в 85% случаев выявляется наличие протрузий, величина которых варьирует от 4 до 7 мм. Считается, что выпячивание дисков становится клинически значимым при размерах более 3 мм. (7), однако другие авторы считают, что объем и характер, выявляемых в просвете позвоночного канала шейного отдела грыж диска, не определяет выраженность и остроту развития клинической симптоматики заболевания.
Протрузии межпозвонковых дисков представляют собой выпячивания фиброзного кольца за края тела позвонка и по всей его окружности (диффузная протрузия) или только части ее (локальная протрузия). Грыжа межпозвонкового диска является результатом смещения и выдавливания пульпозного ядра из своего ложа. Грыжевые массы образуют локальное выпячивание по краю межпозвонкового диска.
Следует дифференцировать локальные протрузии от локальных грыжевых выпячиваний. Локальная протрузия диска, как правило, больше по протяженности, чем грыжевое выпячивание. Кроме того, дифференциальное значение имеют непрямые симптомы грыж диска, к которым относятся облитерация эпидурального пространства, уменьшение плотности дорсальной части диска, асимметрия или изменение положения выходящих нервных корешков.
При наличии задних грыж диска важно отметить деформацию переднего контура дурального мешка, которая может быть обусловлена давлением от локального выпячивания диска или дополнительными структурами, облитерирующими эпидуральное пространство. Вероятно, симптом облитерации эпидурального пространства имеет решающее клиническое значение, так как в этом случае само локальное выпячивание непосредственного влияния на дуральный мешок не оказывает (7). Однако в механизме дискогенного корешкового синдрома наряду с компрессионным фактором важная роль принадлежит и вторичным изменениям в окружающей пораженный диск ткани (отек, гиперемия, реактивное воспаление, спайки и рубцы, артериальные и венозные дисциркулярные нарушения).
Одним из врожденных патологических состояний краниовертебральной области является аномалия Арнольда – Киари, проявляющаяся наличием приступов системного головокружения, тяжестью в голове, головной болью (в затылочной области), неустойчивостью в позе Ромберга, нарушением координации, ухудшением слуха, ушным шумом (как правило с одной стороны), снижением чувствительности роговицы и слизистой оболочки носа, часто – нарушением обоняния и вкуса. По некоторым данным, патология Киари выявляется у 26% больных с подозрением на различные патологические изменения ШОП и кранио-спинальные опухоли (3). Симптоматика аномалии Арнольда – Киари патогенетически обусловлена сдавлением каудальных отделов спинного мозга, позвоночной и мозжечковой артерии смещенными миндалинами мозжечка более чем на 3 мм ниже плоскости большого затылочного отверстия (линии Чемберлена). Следует отметить, что не все случаи расположения миндалин мозжечка ниже линии Чемберлена сопровождаются развитием клинических проявлений. Опускание миндалин мозжечка при патологии Киари составляет 3 – 29 мм (22, 23).
Поскольку, головокружение является симптомом многих соматических и эндокринологических заболеваний, в план обследования включается комплексное исследование соматического, отоневрологического и неврологического (в том числе вегетативного) статуса, лабораторная и рентгенологическая диагностика.
В клинической практике при обследовании больного с кохлеовестибулярными нарушениями нередко ограничиваются лишь рентгенограммой шейного отдела позвоночника, однако, этого недостаточно – 40% пациентов с изменениями на рентгенограммах не имели характерных клинических проявлений и еще 40% больных имели клиническую симптоматику без рентгенологической (7). Поэтому для постановки правильного диагноза и выбора лечебной тактики необходимо применение по крайней мере функциональной рентгенографии (боковая проекция с полным сгибанием и разгибанием головы при сидячем положении больного) (Дадашева М. Н.). Для более точного исследования шейного отдела позвоночника следует прибегать к магнитно-резонансной томографии (МРТ) и магнитно-резонансной ангиографии (3, 9, 11, 24) – самым современным неинвазивным методам нейровизуализации. Преимуществом МРТ является многоплановость изображения, визуализация мягкотканых структур, что позволяет оценить состояние дурального пространства спинного мозга (3, 11). Особенно ценно, что МРТ дает возможность оценить степень пролабирования межпозвонковых грыж, дегенеративные изменения спинного мозга, сужение вертебробазилярных сосудов или их окклюзию, еще до клинических проявлений (27) в виде головокружения, помутнения сознания, наличия патологического позиционного нистагма (24).
Следует отметить, что компьютерная томография дает одноплоскостное изображение, кроме того, ее надежность при исследованиях шейного отдела позвоночника составляет 50% (3).
Целесообразно разделять патогенетическую терапию вертеброгенного головокружения в острый период и период ремиссии, а также на терапию синдрома позвоночной артерии и терапию цервикального синдрома. Терапия синдрома позвоночной артерии включает применение вестибулолитических средств и вазоактивных препаратов, нормализующих гемодинамику. Для нормализации метаболических процессов используются ноотропные лекарственные средства, повышающие устойчивость ткани головного мозга к гипоксии, снижающие выраженность когнитивных и вегетативных расстройств. С целью регуляции обменных процессов целесообразно использование церебролизина. Терапия цервикального синдрома включает купирование болевого синдрома и мышечного напряжения нестероидными противовоспалительными препаратами. Для снижения мышечного тонуса используют миорелаксанты. Витамины группы В рекомендуются для стимуляции обменных процессов. При выраженном психоэмоциональном напряжении и для купирования вегетативного криза возможно применение малых транквилизаторов. В период ремиссии для лечения цервикального синдрома назначают хондропротекторы.
В современной клинической практике больным шейным остеохондрозом с кохлео-вестибулярным синдромом проводится, как правило, курс массажа шейно-воротниковой зоны и надплечий, лечебная гимнастика, фонофорез с новокаином, эуфиллином или гидрокортизоном, электротерапия, магнитотерапия, аэрозоль- и электроаэрозольтерапия, гидробальнеотерапия, рефлексотерапия – корпорально-аурикулярная акупунктура и массаж игольчатым молоточком шейно-воротниковой зоны, позволяющие улучшить кровообращение в вертебро-базилярной системе.
Курс классического, аппаратного, вакуумного или гидромассажа массажа шейно-воротниковой зоны, богатой рецепторами, с охватом паравертебральных областей состоит из 15-20 процедур. Наряду с миорелаксирующим действием, массаж способствует улучшению кровообращения, в частности усилению венозного оттока.
Многие авторы считают, что лечение больных с грыжами, протрузиями, вертеброгенным поражением позвоночной артерии наряду с применением вазоактивных препаратов должно и может включать мануальную терапию (МТ), эффективность которой достаточно высока. Уже после одной – двух процедур МТ (постизометрическая релаксация тонически напряженных мышц и мобилизация соответствующих позвоночно-двигательных сегментов в сочетании с медикаментозным лечением) у 25 больных купировалась субъективная и объективная симптоматика, а после 4 – 6 сеансов МТ все больные (проведено лечение 47 человек) отмечали улучшение состояния, повышалось пульсовое кровенаполнение в вертебро-базилярном бассейне, нормализовывался венозный отток (10). После курса мануальной терапии у большинства пациентов (69,2%) уменьшается частота и длительность приступов головокружения, спонтанный нистагм исчезает в 39,9% случаев, более быстрый регресс симптомов отмечается у больных с блокированием верхне-шейных сегментов (особенно С0 – С1) (6), уменьшается выраженность вегето-сосудистой дисфункции, развивающейся на фоне дегенеративных изменений позвоночника.
Отбор пациентов для проведения МТ должен быть тщательным, поскольку при некоторых формах дегенеративных заболеваний позвоночника МТ может спровоцировать ухудшение состояния больного. При проведении мануальной терапии больным шейным остеохондрозом могут возникать такие осложнения, как нарушение кровоснабжения мозга в вертебробазилярной системе; вегето-сосудистые кризы; компрессия спинного мозга на уровне шейного отдела; формирование нестабильности сегментов шейного отдела.
В связи с возможностью возникновения осложнений мануальную терапию шейного отдела позвоночника необходимо проводить с осторожностью, без каких-либо попыток глубокого массажа. Перед началом курса необходимо исключить у пациента наличие врожденных аномалий развития и системных заболеваний позвоночника, чрезмерную подвижность позвоночных сегментов, сосудистых нарушений системы кровообращения спинного мозга, спондилеза III степени, остеопороза позвоночника разной этиологии, тяжелых заболеваний внутренних органов, воспалительных процессов позвоночника, онкологических заболеваний, состояния после травматических повреждений и хирургических вмешательств на позвоночнике (12).
Уменьшению выраженности головокружения, нормализации функции равновесия способствует включение в комплекс лечебных мероприятий 10-12 сеансов вестибулярной реабилитации (гимнастики), проводимой на стабилографических (/постурографических) комплексах.
Нами проведено обследование и лечение 48 больных с головокружением на фоне остеохондроза шейного отдела позвоночника. При проведении МРТ шейного отдела позвоночника 32 больным (в возрасте от 20 до 63 лет) с трудно поддающейся лечению вестибулопатией и дегенеративными заболеваниями ШОП выявлено наличие грыж диска – у 13, протрузий – у 15, сочетание грыжи и протрузии – у 4, сочетание с аномалиями развития сосудов вертебро-базилярной системы – у 2 пациентов. Показаниями к проведению МРТ были следующие рентгенологические признаки: снижение высоты межпозвонкового диска, наличие остеофитов – костных разрастаний по краям тел позвонков, унковертебрального артроза.
Все пациенты получали медикаментозную терапию, массаж шейно-воротниковой зоны и лечебную гимнастику для больных остеохондрозом, по показаниям мануальную терапию (28 человек) и вестибулярную реабилитацию на постурографическом комплексе (21 человек). В результате проведенного лечения у всех пациентов достигнута компенсация вестибулярной функции в покое, уменьшение длительности и частоты приступов головокружения, улучшение стабилографических показателей.
Таким образом, целенаправленное и рациональное использование всех медикаментозных и немедикаментозных лечебных мероприятий способствует более успешному лечению головокружения.